5. Пакет з навішуванням закрити, помістити в прилад (піднявши верхню плиту не вище ніж під кутом 45°) і висушити протягом 5 хв. при 150…152 °С. Перші 30…50 с верхню плиту (щоб уникнути розриву пакетів) тримати дещо підведеною, потім опустити. Одночасно можна висушувати два пакети.
6. Висушені пакети охолодити в ексикаторі (3…5 хв), після зважити і визначити кількість вологи (%) по формулі:
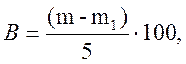
де В - вміст вологи в сирі (%); т - маса паперового пакету з сиром до висушування (г); т1 - маса паперового пакету з сиром після висушування (г); 5 — навішування сиру (г).
7. Щоб визначити вміст сухої речовини (%) в сирі, треба відняти з 100 вміст вологи у відсотках
Приклад. Навішування сиру 5 г; m = 11,4 г; m1= 8,2 г.
11,4-8,2
В = ------------- = 64 %.
5
Вміст сухої речовини: 100 - 64 = 36 %.
Розбіжність між паралельними визначеннями повинна бути не більш 0,5%.
Техніка визначення вологи в сирі експрес-методом (висушування при 160—165 °С).
1. Фарфорову чашку з скляною паличкою і 20-25 г піску помістити в сушильну шафу на 1 г при температурі 102…105 °С.
2. Не охолоджуючи чашку, поставити її на трикутник, що знаходиться на вагах, і зважити.
3.
Відважити в чашку 5 г сиру і ретельно перемішати його з піском, після чого чашку на 20 хв помістити в сушильну шафу
при температурі 160…165 °С. Потім, не охолоджуючи чашки, помістити її на
трикутник і зважити.
4. Обчислити по формулі кількість вологи в сирі
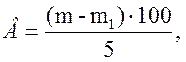
де В - вміст вологи в сирі (%); т - маса чашки з трикутником, піском, скляною паличкою і сиром до висушування (г); т1 — маса чашки з трикутником, піском, скляною паличкою і сиром після висушування (г); 5 - навішування сиру (г).
Приклад, т = 80,1 г; ту = 77,1 г; наважка сиру 5 г
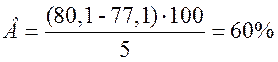
Визначення вмісту солі в солоних сирних виробах без попереднього озоления за допомогою азотнокислого срібла. Суть методу полягає в титруванні екстракту азотнокислим сріблом; по кількості витраченого на титрування азотнокислого срібла розраховують вміст в продукті солі.
Приготування розчину азотнокислого срібла. Відважити 2,906 г азотнокислі срібло з точністю до 0,0002 г. Наважку помістити в мірну колбу на 100 см3, попередньо заповнену на 2/3 дистильованою водою. Обертанням колби перемішати вміст до повного розчинення реактиву, долити дистильованою водою до мітки і ретельно переміщати. Один см3 виготовленого розчину азотнокислого срібла відповідає 0,001 г хлористого натрію.
Техніка визначення.
1. Зважити 5 г продукту, помістити в стакан з носиком місткістю 100…150 см3, підлити 50 см3 дистильованої води, що має температуру 90 °С. Продукт ретельно розтерти скляною паличкою і перенести в мірну колбу на 100 см3 (обполіскуючи стакан дистильованою водою температурою 70…80 °С).
2. Вміст мірної колби охолодити до 20 °С, доливаючи дистильовану воду до мітки, профільтрувати через паперовий фільтр (фільтрат повинен бути прозорим, при необхідності фільтрувати двічі).
3. В конічну колбу піпеткою відміряти 50 см3 фільтрату, додати 5-8 крапель 10%-ного розчину хромовокислого калія і відтитрувати азотнокислим сріблом до слабкого цегляно-червоного кольору, не зникаючого при збовтуванні і подрібненні паличкою великих частинок осаду.
4. Розрахувати вміст солі (З %) по формулі
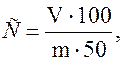
де V - кількість розчину азотнокислого срібла (см3), витраченого на титрування 50 см3 фільтрату; т - маса продукту (г).
Розбіжності між паралельними визначеннями не повинні перевищувати 0,2 %.
Приклад. Натитрування 50 см3 фільтрату витрачено 1,5 см3 азотнокислого срібла, наважка продукту 5 г. Розрахувати вміст солі в сирі.
1,5 • 100
С =---------- = 0,6 %.
5 -50
Чинники, що впливають на точність аналізу
1. Ретельність розтирання продукту і температура води.
2. Точність приготування реактивів.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.