При фазовом переходе жидкость – пар в точке "f" наблюдается значительное возрастание объемной координаты. Число возможных конфигураций многократно возрастает, поскольку межатомное расстояние увеличивается на три порядка.
Сравнительная природа твердой и жидкой фаз рассматривается, с позиции
дефектов кристаллической решетки: точечных, линейных и поверхностных. В жидких
металлах расположение атомов почти такое же плотное, как и в твердом, величина
межатомных расстояний почти такая, как и в твердом. Но в жидкости число
дефектов сопоставимо с числом узлов кристаллической решетки (рис. 16). Потенциальная
энергия атомов имеет минимумы, отвечающие геометрическому расположению атомов в
узлах решетки, а также в местах расположения дефектов. В твердом металле число
дефектов таково, что один дефект приходится на 106 атомов, а в
жидком число дефектов почти такое же, как число атомов. Переход атома из одного
положения в другое в твердом металле обусловлен преодолением энергетического
барьера ![]() , а в жидком величина энергетического
барьера
, а в жидком величина энергетического
барьера ![]() значительно меньше, что и обусловливает многократно
меньшие величины напряжений сдвига у жидких металлов по сравнению с твердыми.
Однако, общеизвестен факт, что при больших скоростях деформации в жидкостях
напряжения сдвига многократно возрастают и становятся сопоставимыми с твердыми
(удар о поверхность воды при большой скорости подобен удару о твердое тело).
значительно меньше, что и обусловливает многократно
меньшие величины напряжений сдвига у жидких металлов по сравнению с твердыми.
Однако, общеизвестен факт, что при больших скоростях деформации в жидкостях
напряжения сдвига многократно возрастают и становятся сопоставимыми с твердыми
(удар о поверхность воды при большой скорости подобен удару о твердое тело).
|
|
Рис. 16. Величины потенциальных энергий для твердого и жидкого металла:
а – потенциальная энергия межатомного взаимодействия твердого металла;
б – потенциальная энергия межатомного взаимодействия жидкого металла;
dA – межатомное расстояние в кристаллической решетке металла;
х – дефект кристаллической решетки
1.7.1. Две модели жидкого состояния металлов
Среди множества моделей жидкостей металлам в большей степени отвечают две: модель ячеек и модель кластеров.
Существо модели ячеек заключается в том, что в жидком металле каждый атом значительную часть времени движется в некоторой области, ограниченной соседними атомами, – ячейки. Предполагается, что каждый атом движется независимо и потенциальная энергия системы (ячейки) равна сумме потенциальных энергий отдельных атомов. Частично ячейки перекрывают друг друга, таким образом, что один и тот же атом может принадлежать разным ячейкам (рис. 17) и при этом расположение атомов в ячейке близко к строению кристаллической решетки металла. Течение жидких металлов рассматривается как перекатывание ячеек (чисто механическое явление по рис. 17) с заменой части атомов в ячейках.
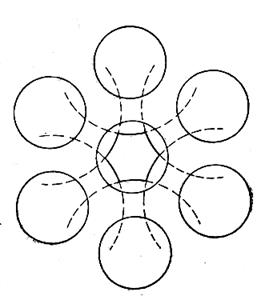
Рис. 17.
По кластерной модели строения жидких металлов полагают, что в расплаве имеется множество микроскопических объемов, в которых имеет место правильное взаимное расположение атомов, подобное расположению атомов в кристаллической решетке конкретного металла. Кластер ("сгусток") – это группа атомов в расплаве с квазикристаллическим строением. Каждый кластер окружен атомами с хаотичным геометрическим расположением. В то же время кластер не представляет собой частицу твердой фазы ввиду чрезмерно малого объема и не имеет соответственно межфазной границы. Кластеры находятся постоянно в динамике образования и разрушения путем псевдоплавления и псевдозатвердевания (рис. 18). С повышением температуры расплава преобладают процессы псевдоплавления, уменьшается число кластеров и их объем. С понижением температуры расплава преобладающая роль становится за псевдозатвердеванием. При достижении температуры затвердевания (ликвидуса для сплавов) часть кластеров достигает размеров кристаллических зародышей.
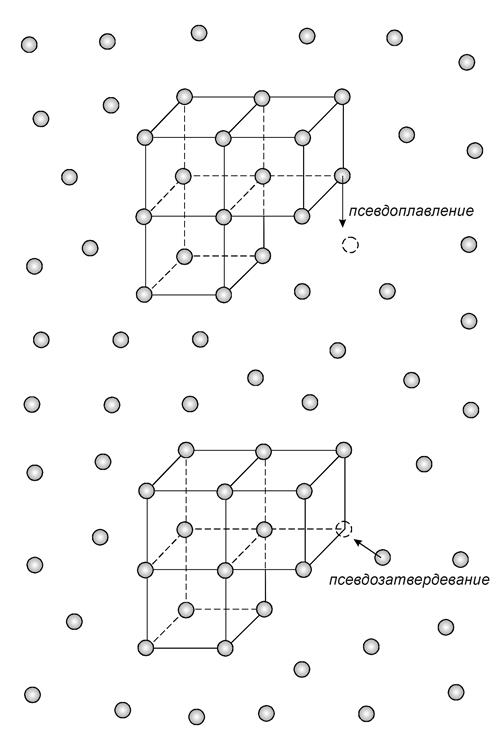
Рис. 18. Модель кластеров жидкого металла
Кластерная модель более логично объясняет свойства и поведение жидких сплавов, в состав которых входят элементы с большой разницей в температурах плавления, например, стали легированные вольфрамом и молибденом, алюминиевокремниевые сплавы. Модель ячеек более подходит к строению расплавов чистых металлов и сплавов, содержащих элементы с близкими температурами плавления.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.