Быстрое охлаждение, перемешивание раствора, высокая температура и небольшая молярная масса растворенного вещества способствует образованию зародышей и получению мелких кристаллов. При возрастании скорости охлаждения расплава скорость образования зародышей вначале растет, а затем падает; поэтому при очень быстром охлаждении расплавов можно избежать зародышеобразование и получить вещество в стеклообразном состоянии. Выращивание крупных монокристаллов производят из метастабильных растворов и расплавов, вводя в них затравочные кристаллы и предотвращая самопроизвольную массу кристаллизации.
Мелкие кристаллы содержат меньше примесей, чем
крупные; последние, однако, легче отделяются от раствора. Если примесь образует
с кристаллами твердый раствор и при этом ее концентрация незначительна, то
распределение примесей между жидкой (или газовой) фазой и образующимися
кристаллами в условиях равновесия кристаллы ![]() раствор
(пар) характеризует коэффициент сокристаллизации:
раствор
(пар) характеризует коэффициент сокристаллизации:
![]() (8), где
(8), где ![]() и
и ![]() –
мольные доли основного вещества и примесей в твердом растворе соответственно,
–
мольные доли основного вещества и примесей в твердом растворе соответственно,
![]() и
и ![]() –
моляльность основного вещества и примеси в жидкой фазе.
–
моляльность основного вещества и примеси в жидкой фазе.
Если ![]() , происходит очистка основного вещества от
примеси, если же
, происходит очистка основного вещества от
примеси, если же ![]() , кристаллы обогащаются примесью.
, кристаллы обогащаются примесью.
|
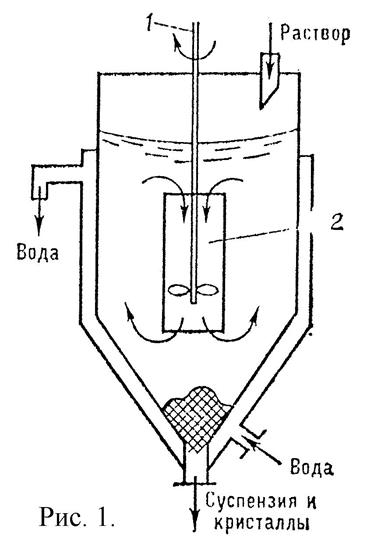
1 – мешалка, 2 – циркуляционная труба Рисунок 15 – Кристаллизатор с мешалкой и водяной рубашкой |
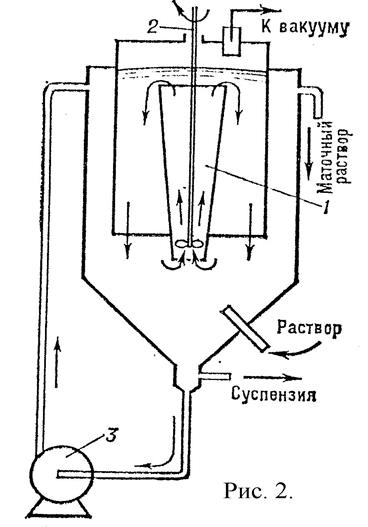
1 – циркуляционная труба, 2 – мешалка, 3 – циркуляционный насос. Рисунок 16 – Циркуляционный вакуум-кристаллизатор |
||||
|
1 – барабан, 2 – ножевое устройство, 3 – приемный бункер, 4 – слой закристаллизовавшегося расплава, 5 – рубашка Рисунок 17 – Барабанный кристаллизатор |
|||||
Для получения особо чистых
веществ производят их многократную перекристаллизацию (смотреть
кристаллизационные методы разделения смесей); при этом, чем меньше ![]() , тем меньше требуется повторных операций.
Используют также аддуктивную (клатратную) и экстрактивную кристаллизацию. В
первом случае в раствор вводят вещество, образующее с примесью клатрат,
выделяющийся при кристаллизации. При экстрактивной кристаллизации в нагретый
концентрированный раствор очищаемого вещества вводят охлажденный экстрагент, не смешивающийся с
раствором и являющийся также хладагентом. Примесь концентрируется
преимущественно в экстрагенте и выводится с ним из кристаллизатора.
, тем меньше требуется повторных операций.
Используют также аддуктивную (клатратную) и экстрактивную кристаллизацию. В
первом случае в раствор вводят вещество, образующее с примесью клатрат,
выделяющийся при кристаллизации. При экстрактивной кристаллизации в нагретый
концентрированный раствор очищаемого вещества вводят охлажденный экстрагент, не смешивающийся с
раствором и являющийся также хладагентом. Примесь концентрируется
преимущественно в экстрагенте и выводится с ним из кристаллизатора.
Кристаллизация производится в кристаллизаторах и может быть непрерывной (при производительности не менее 0,5 т/сут) или периодической. Наиболее распространена кристаллизация при охлаждении растворов и непрерывном их перемешивании (рисунок 15). Кристаллизация при испарении растворителя осуществляется в вакуум-кристаллизаторах (рисунок 16). Кристаллизацию из расплавов часто производят в барабанных кристаллизаторах со съемом осадка с помощью ножей (рисунок 17).
Электрокристаллизация – это переход вещества из ионизированного состояния в растворе или расплаве в кристаллическое в результате электрохимической реакции. Лежит в основе всех процессов электроосаждения металлов, а также формирования слоев оксидов и труднорастворимых соединений на аноде (например, при образовании электролитических защитно-декоративных покрытий, в производстве химических источников тока). Отличается от обычной кристаллизации из пара или раствора тем, что построению кристаллической структуры предшествует перенос заряда с электрода на ион или оба эти акта протекают одновременно. Возникновение зародышей новой фазы при электрокристаллизации требует определенного пересыщения, которое определяется перенапряжением на электроде. Чем выше перенапряжение, тем большее число зародышей возникает в единицу времени на данной площади. Зародыши разрастаются в результате послойного роста граней. Процесс может идти с образованием двумерных зародышей или по закону слоисто-спирального роста на винтовых дислокациях (см. рост кристаллов). В результате линейного роста кристаллов происходит их слияние с образованием сплошного слоя электролитического покрытия.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.