








![]() , (15)
, (15)
где ![]() -
коэффициент распределения (константа фазового равновесия)
-
коэффициент распределения (константа фазового равновесия) ![]() -го компонента при температуре и
давлении наверху колонны;
-го компонента при температуре и
давлении наверху колонны; ![]() - мольная доля
компонента в паре на верху колонны, в случае полной конденсации пара в
дефлегматоре
- мольная доля
компонента в паре на верху колонны, в случае полной конденсации пара в
дефлегматоре ![]() ; q – число
компонентов системы.
; q – число
компонентов системы.
Температура внизу колонны ![]() определяется из уравнения изотермы
жидкой фазы:
определяется из уравнения изотермы
жидкой фазы:
![]() ; (16)
; (16)
где ![]() -
коэффициент распределения
-
коэффициент распределения ![]() -го компонента при
температуре и давлении низа колонны.
-го компонента при
температуре и давлении низа колонны.
Если сырье поступает в колонну при
температуре начала кипения смеси, т.е. доля отгона сырья на входе в колонну ![]() равна нулю, температура сырья
равна нулю, температура сырья ![]() определяется по уравнению изотермы
жидкой фазы (16). Если сырье поступает в колонну при температуре конца кипения
смеси, доля отгона сырья на входе в колонну
определяется по уравнению изотермы
жидкой фазы (16). Если сырье поступает в колонну при температуре конца кипения
смеси, доля отгона сырья на входе в колонну ![]() равна
единице, температура сырья
равна
единице, температура сырья ![]() определяется по
уравнению изотермы паровой фазы (15). Если сырье поступает в колонну в виде
парожидкостной смеси, т.е.
определяется по
уравнению изотермы паровой фазы (15). Если сырье поступает в колонну в виде
парожидкостной смеси, т.е. ![]() , температура
сырья на входе в колонну
, температура
сырья на входе в колонну ![]() определяется из
уравнения:
определяется из
уравнения:
![]() ; (17)
; (17)
или
![]() ;
(18)
;
(18)
где ![]() -
коэффициент распределения
-
коэффициент распределения ![]() - го компонента при
температуре и давлении в зоне питания колонны.
- го компонента при
температуре и давлении в зоне питания колонны.
Уравнение (17) лучше использовать для значений доли отгона, больших 0,5; а уравнение (18) дает лучшие результаты при значениях доли отгона, меньших 0,5.
Коэффициенты распределения ![]() зависят от температуры, поэтому
уравнения (15) – (18) при расчете температур
зависят от температуры, поэтому
уравнения (15) – (18) при расчете температур ![]() решаются
методом последовательных приближений.
решаются
методом последовательных приближений.
1.4. Построение диаграммы фазового равновесия в координатах
y – x
В процессах простой перегонки и ректификации равновесные концентрации фаз определяются зависимостью:
![]() , (19)
, (19)
где ![]() -
мольная концентрация
-
мольная концентрация ![]() - го компонента в паре,
равновесном с жидкостью состава
- го компонента в паре,
равновесном с жидкостью состава ![]() .
.
В случаях, когда разделяемую смесь
можно считать идеальной, т.е. для всех компонентов смеси выполняется закон
Рауля, коэффициент распределения ![]() рассчитывается как
отношение давления насыщенного пара компонента
рассчитывается как
отношение давления насыщенного пара компонента ![]() при
фиксированной температуре к общему давлению в системе
при
фиксированной температуре к общему давлению в системе ![]() :
:
![]() . (20)
. (20)
Для идеальных смесей зависимость между равновесными составами фаз выражается уравнением Рауля-Дальтона:
![]() . (21)
. (21)
Для многих жидких
смесей расчет коэффициента распределения можно производить по уравнению (20),
если общее давление в системе ![]() (5 ат)м.
(5 ат)м.
Давления
насыщенных паров индивидуальных веществ ![]() или
зависимости для их расчета приведены в работах [1-6].
или
зависимости для их расчета приведены в работах [1-6].
Для бинарных
смесей, подчиняющихся закону Рауля, диаграмму фазового равновесия в координатах
y-x (рис. 1.2) строят по следующему
алгоритму. Температурный режим выкипания разделяемой смеси определяется как разность
температур кипения чистого низкокипящего ![]() и
чистого высококипящего
и
чистого высококипящего ![]() компонентов при выбранном
давлении в системе
компонентов при выбранном
давлении в системе ![]() . В этом интервале от
. В этом интервале от ![]() до
до ![]() принимается
ряд значений температуры (обычно десяти значений бывает достаточно). Для каждой
температуры определяются значения давления насыщенных паров компонентов
принимается
ряд значений температуры (обычно десяти значений бывает достаточно). Для каждой
температуры определяются значения давления насыщенных паров компонентов ![]() и рассчитываются из соотношения (20)
коэффициенты распределения низкокипящего компонента. Мольная концентрация
низкокипящего компонента
и рассчитываются из соотношения (20)
коэффициенты распределения низкокипящего компонента. Мольная концентрация
низкокипящего компонента ![]() в жидкости,
кипящей при выбранной температуре и давлении
в жидкости,
кипящей при выбранной температуре и давлении ![]() ;
рассчитывается из соотношения
;
рассчитывается из соотношения
![]() , (22)
, (22)
где ![]() ,
, ![]() - давления насыщенных паров
соответственно высококипящего и низкокипящего компонентов.
- давления насыщенных паров
соответственно высококипящего и низкокипящего компонентов.
После этого из соотношения (21)
определяется мольная концентрация низкокипящего компонента в паре ![]() , равновесном с жидкостью. Далее
строится диаграмма фазового равновесия в координатах y-x ( рис. 1.2).
, равновесном с жидкостью. Далее
строится диаграмма фазового равновесия в координатах y-x ( рис. 1.2).
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()


![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
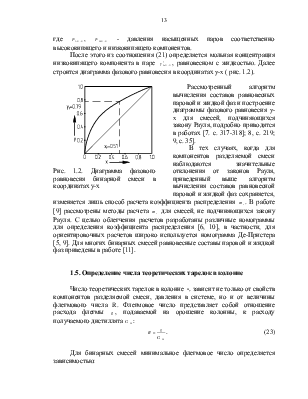
![]() Рис. 1.2.
Диаграмма фазового равновесия бинарной смеси в координатах у-х
Рис. 1.2.
Диаграмма фазового равновесия бинарной смеси в координатах у-х
Рассмотренный алгоритм вычисления составов равновесных паровой и жидкой фаз и построение диаграммы фазового равновесия y-x для смесей, подчиняющихся закону Рауля, подробно приводятся в работах [7. с. 317-318]; 8, с. 219; 9, с. 35].
В тех случаях, когда для компонентов разделяемой смеси наблюдаются значительные отклонения от законов Рауля, приведенный выше алгоритм вычисления составов равновесной паровой и жидкой фаз сохраняется,
изменяется лишь способ расчета коэффициента распределения
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.