Витамин С – жизненно важное соединение, чьи биологические функции связаны с участием в биосинтезе стероидов и реакциях гидроксилирования и, в частности, в превращении пролина в оксипролин (биосинтез коллагена). Участвует в биологическом окислении в тканях, синтезе гормонов, предохраняет адреналин от окисления, способствует повышению свертываемости крови и регенерации тканей, влияет на процесс биосинтеза межклеточного вещества — гиалуроновой кислоты.
При недостатке витамина С нарушается обмен в соединительной ткани, понижается проницаемость капилляров, что ведет к кровоизлияниям и цинге.
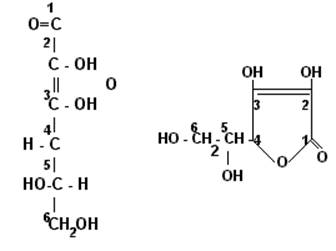 |
Аскорбиновая кислота обратимо переходит в дегидроформу:
![]()
![]()
![]()
![]() O O
O O
![]()
![]() C C
C C
![]()
![]() НО-С
О = С
НО-С
О = С
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
НО-С О - 2H О = С О
![]()
![]()
![]()
![]()
![]()
![]() H-C + 2H H-C
H-C + 2H H-C
HO-C-H HO-C-H
![]()
![]()
СH2-OH СH2-OH
L-аскорбиновая Дегидроаскорбиновая кислота кислота
(восстановленная форма) (окисленная форма)
Ввиду наличия в молекуле двойной связи возможно существование геометрических цис- и транс-изомеров кислоты аскорбиновой. Однако пока известен только один из них – цис-изомер. Два ассиметрических атома углерода обусловливают существование четырех оптических изомеров. Все они получены синтетически, однако только l-изомер является физиологически активным.
Существование витамина С было доказано в результате научных экспериментов на морских свинках в 1907 – 1912 гг. Эти работы показали, что известное с давних времен заболевание цинга вызывается отсутствием в пище некоторого фактора, который получил название антицинготного (антискорбутного) фактора или витамина С. Химическое строение витамина С было установлено в 1930 – 1932 гг. в результате работ Альберта Сент-Дьерди, Нормана Хэворса и Глена Кинга. В 1933 г. Таудеуш Райхштайн впервые синтезировал аскорбиновую кислоту, используя в качестве исходного продукта L-ксилозу. Промышленное производство аскорбиновой кислоты начато в 1936 г.
Кислоту аскорбиновую можно выделить из растительного сырья, в частности из плодов шиповника. Промышленный способ получения кислоты аскорбиновой основан на сочетании химического и микробиологического синтеза из D-глюкозы. Глюконовая кислота и ее g-лактон – простые продукты окисления (дегидрогенизации) глюкозы. Еще в начале 20-х гг. было налажено производство этой кислоты из глюкозы при участии Asperillus nigeг. Нейтрализация кислоты позволяла получать большой выход продукта. В погруженных культурах за 48 ч. конверсии субстрата он составлял 90%: исследования на полупромышленных установках показали, что если ферментацию вести при повышенном давлении, то выход кислоты за 24 ч. составляет 95% от теоретического при использовании раствора глюкозы с концентрацией 150-200 г/л. Процесс можно вести и в полунепрерывном режиме заново используя мицелий (до 9 раз подряд).
В настоящее время применяют метод синтеза аскорбиновой кислоты, основанный на использовании Gluconobacter (старое название – Acetobacter) suboxydans.
1. На первой стадииD-глюкозу восстанавливают в D-сорбит каталитическим гидрированием. Истользуют никелевые катализаторы.
2. Микробиологическая стадия – окисление D-сорбита до L-сорбозы. D-сорбит подвергают глубокому биохимическому окислению Gluconobacter suboxydans. Фермент, непосредственно осуществляющий процесс окисления – сорбитолдегидрогеназа. Для использования на следующей стадии продукт выделяют в кристаллическом виде.
3. L-сорбозу подвергают ацетонированию (чтобы не допустить окисления четырех гидроксилов).
4. Полученную диацетон L-сорбозу окисляют до диацетонгулоновой кислоты, в присутствии NaOCl и никелевого катализатора.
5. Процесс омыления и лактонизацию 2-кето-L-гулоновой кислоты до кислоты аскорбиновой.
6. Очистка аскорбиновой кислоты пропусканием через колонну активированного угля и кристаллизация.
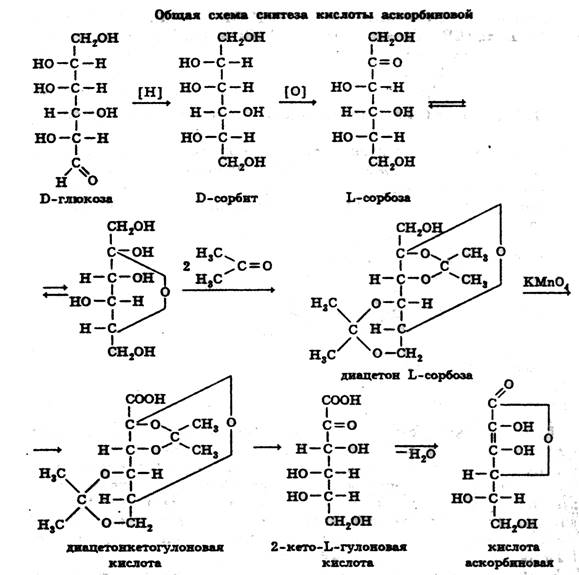 |
Остановимся подробнее на стадии ферментации D-сорбита культурой Gluconobacter suboxydans. Процесс ферментации – аэробный, протекает с выделением энергии и требует постоянного охлаждения. Посевной материал хранится при -70°С. Пересеивают на чашки, либо колбы на 750 мл. с широким отверстием для максимальной аэрации. Чистота исходного материала должна быть не менее 99,5%. Необходима ежедневная проверка на заражение дрожжами. Среда – 77,5% глюкозы (в т.ч. 90% - жидкой и 10% кристаллической), 20% сорбита, 2% остальных сахаров, 0,5% кукурузы (как источник азота и углерода) и NH4PO4. Вода должна отвечать стандартам GLP (good laboratory practice). pH удерживается около 4,0, для чего добавляют уксусную кислоту. В качестве пеногасителей используют олеиновую кислоту и силикон.
Питательную среду стерилизуют одним из двух способов:
1) термическая стерилизация – 10 мин. при 135°С с последующим ступенчатым или непрерывным охлаждением до 37°С;
2) стерилизация фильтрованием;
Воздух очищается прохождением через фильтры с диаметром отверстия 0,8 мм., затем 0,2 мм. и подается вентилятором в ферментер. Непрерывно охлаждается, чтобы поддержать температуру 35°С. Поддерживается избыточное давление, чтобы предотвратить обратный засос воздуха.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.