Известно 2 типа систем, состоящих из ограниченно растворимых жидкостей. В системах первого типа общее давление пара над растворами любого состава больше давлений паров чистых жидкостей при той же температуре (Рº1<P> Pº2). Такая зависимость общего давления пара чистых компонентов и относительно малой взаимной растворимостью жидкостей (анилин-вода)
В системах второго типа общее давление пара над р-рами любого состава лежит между давлениями пара чистых жидкостей при той же температуре (Рº1<P< Pº2) Такая зависимость наблюдается в системах с резко отличающимися давлениями чистых жидкостей и относительно большой взаимной растворимостью жидкостей (никотин-вода).
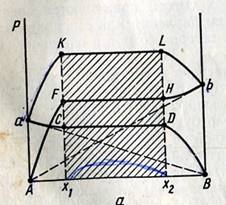
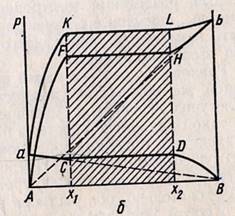
Характер изменения общего и парциальных давлений пара от состава раствора с ограниченной растворимостью жидкостей показана на рис. Заштрихованная область на диаграмме соответствует области расслоения при температуре Т. Пунктирная линия Аb и Ва показан характер изменения парциальных давлений компонентов в системе, подчиняющиеся з-ну Рауля. Кривые аCBD и AFHb изображают изменения парциальных давлений пара компонентов А и В, а кривая аKLb – изменение общего давления пара в зависимости от состава жидких фаз
11.Методы разделения смесей. Ректификация.
Автоматизированный процесс, приводящий к разделению жидкого раствора наз-ся ректификацией.
Разделение смеси ведется в ректификационной калонне.
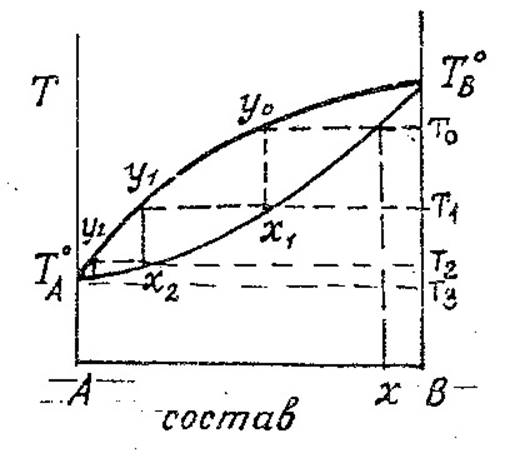
Последовательность разделения сложной смеси у/в можно рассмотреть с помощью диаграммы. В начале жидкость состава х0 нагревается до температуры кипения Т0 .При этой температуре выделяется из жидкости пар состава у0. Этот пар, проходя через патрубок, вступает в контакт с жидкостью (флегмой) на тарелке при Т1<Т0. При конденсации пара состава у0 в жидкости на I-ой тарелке выделяется теплота конденсации, за счет которой из жидкости состава х1 на этой тарелке выделяется пар состава у1. Этот пар обогащен более НК компонентом (у1>y0). Пар состава у0 конденсируется в жидкость состава х1. Пар состава у1 поступает на 2-ю тарелку, где часть его конденсируется в жидкость состава х2, и за счет теплоты конденсации выделяется пар состава у2 при температуре Т2 и.т.д.
Температура в верхней части колонны снижается в ряду :
Т0>T1>T2>T3>T4. Число ступенек на диаграмме температура-состав опред. число тарелок, кот. необходимо разместить в колонне для разделения раствора на отдельные компоненты. Разделяющая способность зависит от относительной летучести компонентов (чем α боьше тем разделение идет лучше ),от конструкции тарелок .
10.Первый з-н Канавалова
Пар над смесью 2х летучих жидкостей относительно богаче тем из компонентов, прибавление которого к смеси повышает общее давление пара при данной температуре или понижает температуру кипения.
Графическое доказательство
На основе рис. Можно показать, что в паровой фазе содержится больше НКК, чем в жидкой фазе, находящейся в равновесии с паровой фазой. Для доказательства этого нагреваем изобарически жидкость состава х1 до температуры кипения Тк. При этой температуре жид-ть испаряется и образуется пар состава у1, который при конденсации образует жидкость состава х2. Из рисунка следует, что у2 > у1, то есть в паровой фазе НКК содержится больше, чем в жидкой фазе. Следовательно, в паре содержится больше того компонента, который кипит при более низкой температуре.
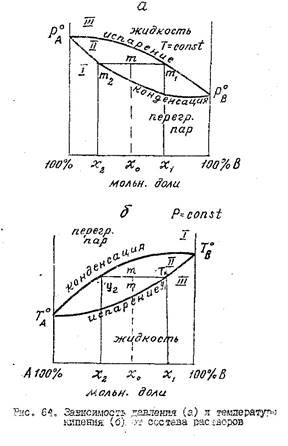
I – область пара, II – область жидкости, III – область равновесия пара и ж-ти.
Термодинамический вывод: исходя из уравнения Гиббса - Дюгема, которое для бинарной смеси жидкостей на небольшом удалении от экстремума можно записать в таком виде.
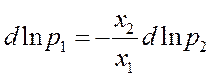
Подставляем в это выражение
Х1=1-Х2 :
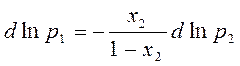
Выделяем из dp1 :
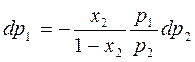
Давление p1 и р2 по з-ну Дальтона можно связать с составом паровой фазы:
р1=(1-у2)Р и р2=у2Р
Подставляем в предыдущее уравнение:
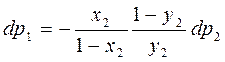
Полное давление по з-ну Дальтона равно сумме парциальных давлений:
Р=р1+ р2
Дифференцируем dP=dp1 +dp2
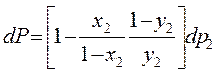
Поделим на dx2
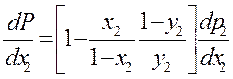
Жидкости, имеющие максимум или минимум на кривых давление -состав соответствуют минимумы и максимумы на кривых Ткип – состав, причем в точках минимума и максимума составы жидкой и паровой фазы равны.
Отклонение свойств реальных растворов от св-в идеальных могут быть настолько большими, что кривые давления насыщенного пара или Ткип в зависимости от состава раствора могут иметь максимум или минимум давлении температуры кипения.
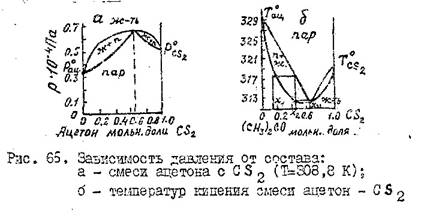 *еще два графика, но наоборот, т.е минимум давление,
максимум температура
*еще два графика, но наоборот, т.е минимум давление,
максимум температура
Максимум на кривых давление – состав появляется у р-ров жидкостей, полиэдры кот. однородного состава более прочны, чем полиэдры разнородного состава, и наоборот. В точках максимума или минимума давлений или Ткип составы жидкой и паровой фаз равны (х=у). Смеси такого состава называются азеатропами или неразделяющимися.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.