МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
Государственное образовательное учреждение высшего профессионального образования
Владимирский государственный университет имени Александра Григорьевича и Николая Григорьевича Столетовых
Кафедра «Химии и химической технологии»
Тема: “ Определение Ph раствора”.
Выполнил:
Студент гр. РЭ-111
А
Проверил: А
Владимир,2011
|
Номер пары пробирок |
Индикатор |
Наблюдаем окраску |
|
|
В сильнокислой среде (pH=1) |
В сильнощелочной среде (pH=13) |
||
|
№1 №1а |
Фенолфталеин |
Бесцветный |
Малиновый |
|
№2 №2а |
Лакмус |
Красный |
Синий |
|
№3 №3а |
Метилоранж |
Красный |
Оранжевый |
Определение рН раствора при помощи индикаторов (визуально-калориметрический метод)
Получить у преподавателя раствор, в котором определить значение водородного показателя рН. Пронумеровать 3 пробирки по номерам имеющихся в вашем распоряжении индикаторов. Поместить в каждую пробирку по 1-2 мл исследуемого раствора и добавить по 1-2 капли каждого индикатора. Отметить цвет раствора в каждой пробирке. Установить порядок величины рН в исследуемом растворе.
Вещество + лакмус ® красный
Вещество + метилоранж®красный
Вещество + фенолфталеин®бесцветный
Вывод: в пробирке кислота pH » 3, среда кислая.
Определение рН раствора при помощи универсальной индикаторной бумаги
Получить у преподавателя раствор, рН которого надо определить. От книжки с универсальной индикаторной бумагой оторвать одну полоску и погрузить ее на несколько секунд в исследуемый раствор. Вынуть полоску и сразу же сравнить окраску сырой бумаги с цветной шкалой. Отметить значение рН, соответствующее данному цвету. Указать характер среды и приблизительно вычислить концентрацию ионов водорода.
С помощью универсальной индикаторной бумаги определили, что pH = 1.
pH= -lg[H+] [H+] =10-1
Определение рН раствора уксусной кислоты на рН-метре
Приготовить 50 мл 0,1 М раствора уксусной кислоты из 1 М уксусной кислоты. Для этого расчетное количество 1 М раствора отобрать пипеткой или мерным цилиндром, перенести в мерную колбу на 50 мл и добавить до метки дистиллированной воды. Приготовленный раствор перелить в стакан на 50 мл и измерить значение рН раствора на рН-метре. Это будет практическое значение рН. Вычислить теоретическое значение рН 0,1 М раствора уксусной кислоты, учитывая, что константа диссоциации уксусной кислоты К= 1,86×10-5. Рассчитать относительную ошибку опыта.
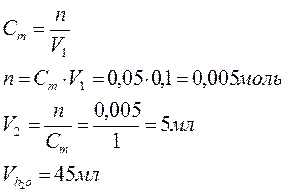
Кдис.= 1,86×10-5
0,1-x x x
СH3COOH Û СH3COO- + H+
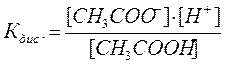
![]()
x2 – 0,186×10-5 +1,86×10-5x = 0
Д=0,00000744
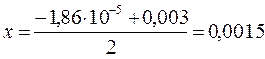
pHтеор. = -lg[H+] » 2,87
pHпр. = 3
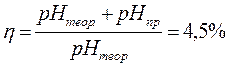
Определение рН раствора гидроксида натрия на рН-метре
Приготовить 50 мл 0,005 М раствора гидроксида натрия из 0,05 М раствора. Для этого расчетное количество 0,05 М раствора отобрать пипеткой или мерным цилиндром, перенести в мерную колбу 50 мл и довести до метки дистиллированной водой. Приготовленный раствор перелить в стакан на 50 мл и измерить рН на рН-метре. Это будет практическое значение рН. Вычислить теоретическое значение рН 0,05 М раствора гидроксида натрия, учитывая, что коэффициент активности этого раствора равен 0,9. Вычислить относительную ошибку опыта.
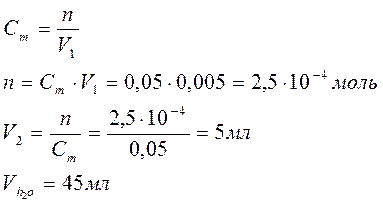
[OH-]=0,05×0,9×1=0,045
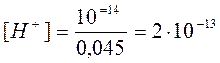
![]()
pHтеор. = 11,7
pHпр. = 11,4
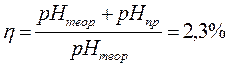
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.