
















КОНЦЕНТРАТЫ, СКОРОПОРТЯЩИЕСЯ И
НЕСТОЙКИЕ ПРЕПАРАТЫ
ТЕМА: «Анализ концентрированных растворов»
ЦЕЛЬ РАБОТЫ. Овладеть методами внутриаптечного контроля качества концентрированных растворов (концентратов)
ЦЕЛЕВЫЕ ЗАДАЧИ: 1.Изучить особенности анализа концентратов в аптечной практике.
2. Провести качественный анализ концентратов фармакопейными и нефармакопейными реакциями.
3. Определить количественное содержание лекарственного вещества в концентратах химическими и физико–химическими методами.
4. Провести расчеты в количественном анализе концентратов:
– фактора пересчета (К); титра (Т);
– допустимых норм расхода титрованного раствора в мл (минимум – максимум);
– содержания вещества в % (Х).
5. Сравнить отклонения лекарственного вещества в концентратах с нормами отклонений по приказу № 305.
6. Сделать вывод о необходимости укрепления или разведения концентрата и провести соответствующие расчеты.
7. Разбавить или укрепить концентраты.
8. Провести повторный количественный анализ.
9. Оформить протокол анализа.
ОБЪЕКТЫ ИССЛЕДОВАНИЯ: Концентрированные растворы:
Аммония хлорида 20 %;
Кислоты аскорбиновой 5 %;
Кислоты борной 3 %;
Натрия гидрокарбоната 5 %;
Натрия тиосульфата 60 %;
Гексаметилентетрамина 10 %.
Концентрированные растворы, приготовленные в аптеках, должны быть проверены на подлинность, плотность и количественное содержание препарата.
В инструктивно–методических указаниях приводятся таблицы, где указывают наименование препарата, концентрацию его в растворе, плотность, реакции подлинности, количественное определение объемным или физико–химическим методом, фактор пересчета (К), нормы раствора титрованного раствора (минимум – максимум с учетом допустимых отклонений) и сроки хранения.
Процентное содержание препарата (Х) в анализируемом растворе определяют по формуле:
Х = К • V,
где К – фактор пересчета;
V – объем израсходованного титрованного раствора.
Фактор пересчета (К) вычисляют по формуле:
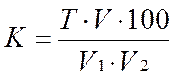 , где
Т – титр соответствующей молярности;
, где
Т – титр соответствующей молярности;
V – объем разведенного раствора, мл;
V1 – объем концентрированного раствора, взятого для разведения, мл;
V2 – объем разведенного раствора, взятого для анализа, мл.
Если после количественного определения установлено, что концентрация раствора не укладывается в соответствующие пределы, то тогда раствор укрепляется или разводится и анализируется повторно.
Формулы расчета для исправления концентрации растворов,
приготовленных массо–объемным или массо–весовым способом
I. Найденная концентрация крепче требуемой:
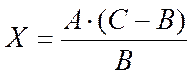 , где X – количество
воды, необходимое для разбавления приготовленного раствора, мл;
, где X – количество
воды, необходимое для разбавления приготовленного раствора, мл;
A – объем приготовленного раствора, мл;
B – требуемая концентрация раствора, %;
C – фактическая концентрация раствора, %.
II. Найденная концентрация слабее требуемой:
1. Для растворов, приготовленных массо–объемным способом.
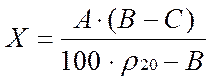 ,
,
2. Для растворов, приготовленных массо–весовым способом.
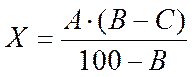 , где X –
количество сухого вещества, которое необходимо добавить к раствору, г;
, где X –
количество сухого вещества, которое необходимо добавить к раствору, г;
A – объем приготовленного раствора, мл
B – требуемая концентрация раствора, %;
ρ20 – плотность раствора при 20 0С, г/см3;
С – фактическая концентрация раствора, %.
· При содержании лекарственного вещества до 20 % – не более ± 2 % от обозначенного процента.
· При содержании лекарственного вещества свыше 20 % не более ± 1 % от обозначенного процента.
Пример расчета отклонений:
При количественном определении 20 % аммония хлорида на титрование теоретически должно быть израсходовано 9,35 мл 0,1 моль/л раствора серебра нитрата.
Расчет отклонений:
9,35 мл составляет 100 %
Х мл составляет ± 2 %
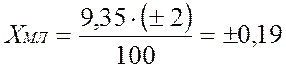
Максимальное отклонение (max)
9,35 + 0,19 = 9,54
Минимальное отклонение (min)
9,35 – 0,19 = 9,16
Пределы отклонений [ 9,16 мл – 9,54 мл ]
ЗАДАНИЕ 1. ПРОВЕСТИ АНАЛИЗ КОНЦЕНТРИРОВАННЫХ РАСТВОРОВ, ПРИГОТОВЛЕННЫХ
МАССО–ОБЪЕМНЫМ СПОСОБОМ
РАСТВОР АММОНИЯ ХЛОРИДА 20 %
1. К 5 - 6 каплям раствора прибавляют 0,5 – 1 мл раствора натрия гидроксида и нагревают. Выделяется аммиак, обнаруживаемый по запаху и посинению красной лакмусовой бумаги.
2. К 2 - 3 каплям раствора прибавляют 2 – 3 капли разведенной азотной кислоты и раствора серебра нитрата. Образуется белый творожистый осадок, растворимый в растворе аммиака.
К 5 мл разведенного раствора (5 : 100) прибавляют 2 мл воды и титруют 0,1 моль/л раствором серебра нитрата до оранжево–желтого окрашивания (индикатор – калия хромат).
РАСТВОРГЕКСАМЕТИЛЕНТЕТРАМИНА 10 %
К 2 - 3 каплям раствора прибавляют 0,01 г салициловой кислоты и 2 – 3 капли концентрированной серной кислоты. Появляется розовое окрашивание.
10 мл разведенного (10 : 100) раствора титруют 0,1 моль/л раствором хлороводородной кислоты до фиолетового окрашивания (индикатор – 2 капли метилового оранжевого и 1 капля метиленового синего.
РАСТВОР КИСЛОТЫ АСКОРБИНОВОЙ 5 %
1. К 4 - 5 каплям раствора прибавляют 2 – 3 капли раствора серебра нитрата; образуется металлическое серебро в виде серого осадка.
2. К 4 - 5 каплям раствора прибавляют 1 – 2 капли гексацианоферрата (III) калия, 2 – 3 капли раствора железа (III) хлорида; появляется синее окрашивание.
1. К 1 мл раствора прибавляют 5 мл воды и титруют 0,1 моль/л раствором
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.