2,13333∙10-5 г 1,066∙10-5 г. 3,2∙10-5 г.
Схема образование муравьиной кислоты следующая 2HCOH + O2 → 2HCOOH (медленная).
64 г/моль 32г/моль 96 г/моль
Количество возможного окисленного формальдегида составит
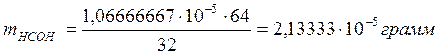 ,
,
а количество образовавшейся муравьиной кислоты равно
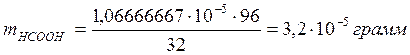 .
.
3 стадия – окисление
муравьиной кислоты кислородом,
образовавшимся в результате разложения пероксида с образованием промежуточного
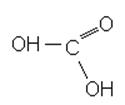
соединения (гидроксо кислоты – CHOОOH).
Процесс протекает по следующей схеме:
(3,2∙10-5 ):2=1,6∙10-5 г. 2,13∙10-5 г – образовалось кислоты
HCOOH + 0,5O2 → 2CHOOOH (быстрая), или
48 г/моль 16 г/моль 64 г/моль
где
количество кислоты составит 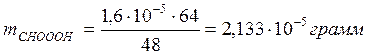
4 стадия – гидроксокислота, как нестойкое соединение образует углекислый газ и воду.
Процесс протекает по следующей схеме:
HCOOOH → CO2 +H2O (быстрая стадия).
Образовавшийся пероксид водорода (H2O2) в количестве m=3,4∙10-5 гграмма на 1
литр, соответствует концентрации ![]() или
или ![]() , может окислить
, может окислить ![]() формальдегида в каждом литре воды
(см. расчёт стадии 2).
формальдегида в каждом литре воды
(см. расчёт стадии 2).
Кинетическое уравнение лимитирующей стадии, процесса третьего порядка, будет иметь вид
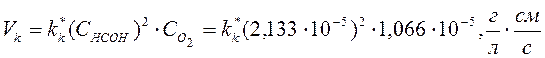 ,
,
где
k* – константа скорости гетерогенного процесса,
изменяющее своё значение от температуры и качества катализатора (k*=f(Kат;T),
![]() – концентрация кислорода, пошедшего
на окисление формальдегида (см. уравнение стадии 2).
– концентрация кислорода, пошедшего
на окисление формальдегида (см. уравнение стадии 2).
Определение температурного интервала и константы скорости процесса при использовании платинированного платинового электрода (Pt/Pt)
При построении графической зависимости (рис.1) lgk* от 1/Т производятся следующие расчёты. По исходным данным энергии активации и температуре определяются углы a1 для построения прямой кинетической области и a2 – для диффузионной:
Табл. 3
Определение угла наклона прямой кинетической области Pt/Pt
|
Эн. актив |
||||||
|
кинет обл |
||||||
|
tga1 |
Eакт(к), кДж/мольК |
R, кДж/мольК |
tg (180=a1) |
arctg(180=a1) |
(180-a1) |
a1 |
|
-7,519E+03 |
143,96 |
8,314 |
7,519E+00 |
1,438569166 |
82,42394176 |
97,57605824 |
Определение угла наклона прямой диффузионной области Pt/Pt
|
Эн. актив |
||||||
|
кинет обл Eакт(к), |
||||||
|
tga2 |
кДж/мольК |
R, кДж/мольК |
tg (180=a2) |
arctg(180=a2) |
180-a2 |
a2 |
|
-9,578E+02 |
18,34 |
8,314 |
9,578E-01 |
0,76387032 |
43,76654546 |
136,2334545 |
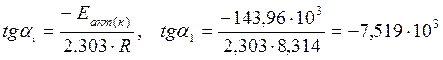 ,
,
или –tga1=tg(180-a1)= 7,519·103, тогда угол (180–a1)=82,43о, a1=97,57о.
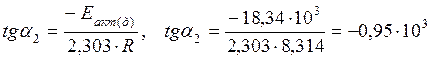 ,
,
или –tga2=tg(180-a2)=0,95·103,
тогда угол (180-a2) = 43,76о,
a2 =
136,23о.
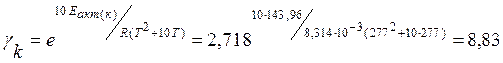
Табл. 4
Температурный коэффициент кинетической области Pt/Pt
|
Темпер. коэф |
e |
Eакт(к) |
R |
T |
|
gк (Pt/Pt) |
2,718281828 |
143,96 |
8,314 |
277 |
|
8,829174908 |
При этом kк* – эффективная
константа скорости гетерогенного процесса кинетической области равна – (lgkк*=0,99
по графику зависимость lgkк* от 1/T), а
kк*= 100,99 = 9,77 см/с. Концентрация окислителя
в водном растворе равна ![]() .
.
По графической зависимости (рис.1) определён температурные интервалы кинетической области, который начинается с температуры 277 К и ниже (рис.1 кривая 1), а температурный интервал диффузионной области начинается с температуры 288 К и выше (кривая 2).
Скорость процесса окисления формальдегида составит
Табл. 5
Кинетическое уравнение лимитирующей стадии (кинетика)
|
Скорость |
Константа |
Концентрация |
Концентрация |
|
протекания (Pt/Pt) |
скорости |
образов. продукта |
образов. O2 |
|
Vk, г/л(см/с) |
k*(k), см/с |
CHCOH, г/л |
CO2,г/л |
|
4,7414E-14 |
9,7700E+00 |
2,1330E-05 |
1,0667E-05 |
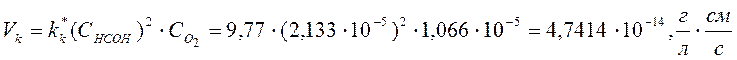 ,
,
что соответствует скорости загрязнения рабочей части платинового электрода.
Температурный коэффициент диффузионной области равен:
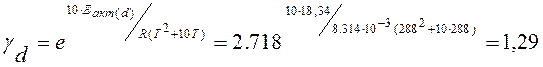
Табл.6
Температурный коэффициент диффузионной области Pt/Pt
|
Темпер. коэф |
e |
Eакт(к) |
R |
T |
|
gd (Pt/Pt) |
2,718281828 |
18,34 |
8,314 |
288 |
|
1,293081426 |
При этом kд* – эффективная константа скорости диффузии равна – (lgkд*=1,32 по графику зависимость lgkд* от 1/T), kд*= 20,89 см/с, а скорость процесса в диффузионной области, начиная с температуры 288 К (15оС) и выше равна:
Табл.7
Кинетическое уравнение лимитирующей стадии (диффузия)
|
Скорость |
Константа |
Концентрация |
Концентрация |
|
протекания (Pt/Pt) |
скорости |
образов. продукта |
образов. O2 |
|
Vд, г/л(см/с) |
k*(д),см/с |
CHCOH,г/л |
CO2,г/л |
|
1,0138E-13 |
2,0890E+01 |
2,1330E-05 |
1,0667E-05 |
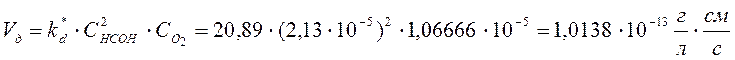
что почти в десять раз быстрее кинетической области.
Зона 3 (температурный интервал 277 – 288 К) является переходной областью (рис.1).
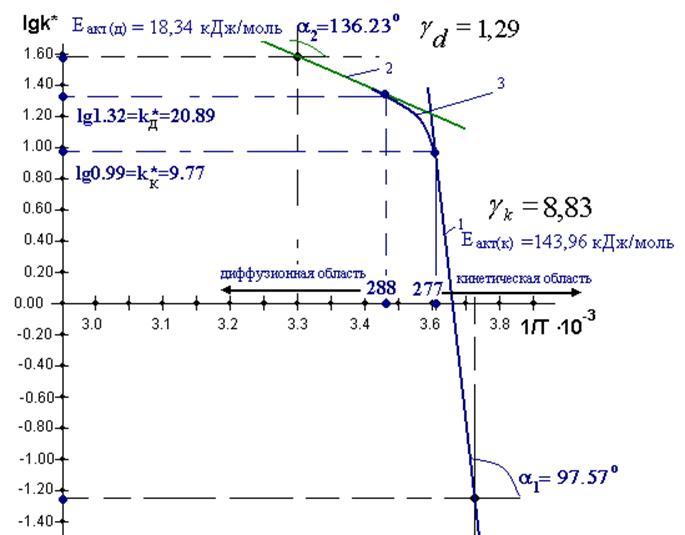
Рис. 1. Зависимость lgk* от 1/T для гетерогенного процесса
Определение количества платиновых платинированных электродов производится с учётом времени (табл.9) и степени очистки водоёма до предельно допустимых величин (ПДК) и его производительности по выходу продукта окисления
.
Excel. лист 3. Табл. 8
Определение количества Pt/Pt электродов
|
nPt/Pt, шт |
kсм |
kэф.очист |
t,c |
Сокисл,г/л |
ПДКHCOH, г/л |
Объём. сточных вод Vст.вод, дм3 |
Объём. водоёма Vвод, дм3 |
Конц.HCOH в сточ водах CHCOH,г/л |
|
5,8746E+00 |
2 |
0,86 |
6,1234E+05 |
2,1333E-05 |
2,0000E-04 |
2,9400E+05 |
3,1000E+07 |
1,9200E-01 |
|
6 штук |
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.