


Задание 6.
Найти Eиkпо заданным результатам опытов на установке, приведенной на рис. 1. Здесь r - радиус сферического сосуда с веществом; U, I - падение напряжения и сила тока в нагревателе на втором этапе опыта.
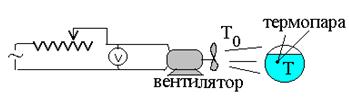
Рис.
1. Схема
установки для изучения теплового взрыва
при теплоотводе
Дано:
|
№ варианта |
DT*,K |
DTtest, K |
I, A |
U,В |
Q, кал/г |
T0,°C(К) |
r,cм |
|
7 |
10 |
20 |
1 |
220 |
500 |
127(400) |
2.0 |
R
= 2![]() ;
;
V=4/3πr3 – объёмсферического сосуда с веществом.
Решение:
q+ = q–, q+ = VQW(T), q– = Sa(T – T0). (1)
q+ = q+test = IU (2)
Математически зажигание или погасание означает одновременное выполнение условий
q+(T)
= q–(T), ![]() =
= ![]()
q+ = VQW(T), q– = Sa(T – T0), W = ke–E/RT.
После подстановки получим:
VQke–E/RT = Sa(T – T0),
VQk e–E/RT(E/RT2) = Sa. (3)
Приравнивая для двух уравнений (3) отношения правых и левых частей, получим уравнение дляТ:
T– T0 = RT 2/E (4)
Уравнение (4) имеет два решения, которые задают значения критических температур зажигания и потухания:
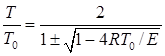 . (4)
. (4)
Учтем, что 4RT0/E << 1, тогда (5) принимает вид
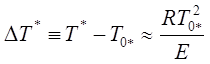 . (6)
. (6)
Тепловой эффект Q для исследуемого вещества известен. В этом случае эксперимент позволяет найти E иk. Энергию активацииЕможно найти уже после первого этапа из формулы (18):
E = RT02/DT*.(7)
Для получения критического условия зажигания подставим уравнение (6) в любое из соотношений (3), например, в первое, и запишем его кратко с использованием обозначений (1) и (6):
q+(Т0* + DТ*) = (Sa)*DТ*. (8)
Для экспоненты в левой части (19) используем разложение Франк-Каменецкого и подставим тудаDТ* из (6), тогда (8) примет вид
q+(Т0*)e = (Sa)*DТ*. (9)
Чтобы найти k, найдем правую часть (9) с использованием данных второго этапа эксперимента. Тепловой баланс для этого этапа (после выхода на стационарный режим) имеет вид
q+=
![]() ,
q+ = q+test,
,
q+ = q+test,![]() =
SaDTtest.(10)
=
SaDTtest.(10)
Так как на втором этапе использовались те же величины (S,T0, U), что и в момент теплового взрыва на первом этапе, можно считать одинаковыми зависящие именно от этих параметров величины (Sa) на первом и втором этапах:
(Sa)*= (Sa)test. (11)
Из (10) находим
(Sa)test = q+test/DTtest. (12)
Подставив (6), (11), (12) в уравнение (9), получим
q+(Т0) e = q+testDT*/DTtest. (13)
Для левой части уравнения (13) используем выражение (1) и равенство W = ke–E/RT, или сразу первое уравнение (3) и применим еще раз (6):
k
= 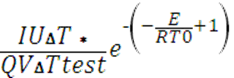 ;
;
∆T* = RT02/E ; -(ET0)/ RT02 +1 = -T0/∆Ttest +1
k
= 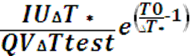 (14)
(14)
Рассчитаем Eиkпо формулам (7) и (14):
E
= 0.2*4002 =3200![]() кал/моль
кал/моль
Для расчёта kпереведём Qв Дж/г:
500![]() =
= 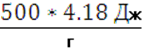 = 2090 Дж/г
= 2090 Дж/г
k
= =
13548999*108
Ответ: E
= 3200кал/моль k = 13548999*108
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.