




самым, искажая аналитический сигнал при определении большинства веществ.
Полярограмма и ее характеристика
Если в электролизер поместить раствор CdCl2 (1-10-3М), фон-раствор КСl (0,1 М), удалить растворенный кислород, подать напряжение на катод и регистрировать изменение тока, протекающего через ячейку, то получим полярограмму – полярографическую волну. Полярограмма имеет три характерных участка (рисунок 4):
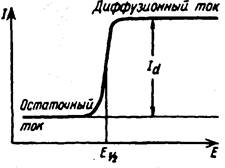 |
Рисунок 4. Полярограмма
1. С момента замыкания цепи через ячейку протекает небольшой ток, называемый остаточным.
2. Затем наблюдается резкое увеличение тока. Потенциал в точке Еv2 называют потенциалом выделения. Он соответствует началу электрохимической реакции восстановления ионов кадмия (II) на электроде с образованием раствора металлического кадмия в ртути (амальгамы): Cd+2 + 2e + Hg ® Cd(Hg).
3. Ток растет, а потом достигает некоторой постоянной величины, называемой предельным током.
Характеристиками полярограммы, связанными с природой восстанавливающегося на электроде вещества и его концентрацией,являются соответственно потенциал полуволны Е1/2 и Iд.Зависимость диффузионного тока от концентрации деполяризатора выражается уравнением Ильковича:
Iд = 607 n D1/2 m2/3 t1/6 с,
где Iд – диффузионный ток, мкА;
n – число участвующих в электрохимической реакции электронов;
D – коэффициент диффузии деполяризатора (количество вещества, диффундирующее в единицу времени через единицу площади при градиенте концентрации, равной единице), см2c-1;
m – скорость вытекания ртути из капилляра, мг/с;
t – время жизни капли, с;
с – концентрация деполяризатора, мл•моль•л-1.
Качественный анализ. В основе качественного полярографического анализа лежит величина потенциала полуволны, характеризующая природу деполяризатора. Это табличная величина, зарегистрировав полярограмму по Е1/2 по таблице определяют вещество. Количественный анализ. Для количественного определения веществ в полярографии используют три способа: метод градуировочного графика, метод стандартов, метод добавок.
Метод градуировочного графика. Регистрируют полярограммы приготовленных стандартных растворов определяемого компонента в одинаковых условиях. Строят градуировочный график в координатах высота волны (или диффузионный ток) – концентрация. В идентичных условиях регистрируют полярограмму анализируемого раствора и, измерив высоту волны, по градуировочному графику находят искомую концентрацию.
Метод стандартов. Сравнение высот волн на полярограммах анализируемого и стандартного растворов, полученные в идентичных условиях.
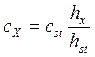 , где сх – концентрация вещества в
анализируемом растворе;
, где сх – концентрация вещества в
анализируемом растворе;
cst – концентрация стандартного раствора;
hx – высота волны на полярограмме анализируемого раствора;
hst – высота волны на полярограмме стандартного раствора.
Метод добавок. После того как полярограмма анализируемого раствора записана, в ячейку добавляют известное количество определяемого вещества и записывают полярограмму раствора с добавкой. Измерив высоты волн на обеих полярограммах, рассчитывают концентрацию определяемого вещества.
Применение. Полярографическим методом можно определять практически все катионы металлов, многие анионы, неорганические и органические вещества. Достоинства метода. Высокая воспроизводимость, хорошая чувствительность метода – 10-8 -10-2 М. Простота конструкции. Широкая область поляризации ртутного электрода. Недостатки: токсичность ртути, хрупкость конструкции, может засориться капилляр.
Метод инверсионной вольтамперометрии
Метод пригоден для определения органических и неорганических веществ вплоть до 10-9...10-10 М [4]. В этом методе используют предварительное концентрирование определяемых компонентов на поверхности индикаторного электрода электролизом, а затем регистрируют инверсионную вольтамперограмму.
Проводят электролиз анализируемого раствора при постоянном перемешивании при потенциале предельного тока самого трудно восстанавливающегося
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.