

Министерство образования Российской федерации
Санкт-Петербургский государственный горный институт
Отчет.
по лабораторной работе:
Фотометрическое определение Железа (III).
Группа АПМ-01
Выполнил: студент Павлов Р. Д.
Проверил: доцент Литвинова Т. Е.
дата: 25.10.02
Санкт-Петербург
2002
1. Цель работы: фотометрическое определение концентрации вещества в растворе по измеренному значению оптической плотности при помощи калибровочного графика, построенного по серии стандартных растворов.
2. Приборы и реактивы:
1. Фотоколориметр КФК-3.
2. Мерные колбы емкостью 50мл - 7 шт.
3. Пипетки, градуированные на 1 и 10 мл.
4. Стандартный раствор соли железа 0,1 г/л.
5. Азотная кислота, разбавленная 1:1.
6. Роданид аммония (или роданид калия), 10% -ный раствор.
7. Рабочий раствор соли железа 0,8 ммоль/л (готовится разбавлением стандартного раствора).
8. Задачи с исследуемым раствором с концентрацией по железу 18 – 30 мг/л.
3. Приготовление рабочего раствора:
Чтобы
получить раствор с концентрацией рабочего, нужно разбавить стандартный в n раз, где n находится
как отношение концентраций стандартного и рабочего раствора: 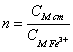 , тогда подставив в эту формулу
известные концентрации, получим -
, тогда подставив в эту формулу
известные концентрации, получим - ![]() .
.
Готовим
7 колб объемом рабочего раствора 0, 1, 2, 4, 6, 8, 10 мл, потом добавляем во
все колбы 1мл азотной кислоты (![]() ), далее добавляем
5 мл роданида аммония (или калия), объем растворов доводим до метки
дистиллированной водой, тщательно перемешиваем.
), далее добавляем
5 мл роданида аммония (или калия), объем растворов доводим до метки
дистиллированной водой, тщательно перемешиваем.
Чтобы измерить оптическую плотность данного вещества, нужно одну из кювет заполнить раствором сравнения, другую – исследуемым раствором, начиная с наименее концентрированного.
|
Объем исследуемого раствора в , мл |
0 |
1 |
2 |
4 |
6 |
8 |
10 |
|
Оптическая плотность исследуемого раствора |
0,000 |
0,073 |
0,129 |
0,317 |
0,544 |
0,806 |
0,908 |
Помещаем кюветы с растворами в прибор, устанавливаем на приборе длину волны 480 нм и считаем оптическую плотность раствора сравнения равной нулю, потом относительно ее измеряем оптическую плотность исследуемого раствора. Так проделываем с растворами всех концентраций. В итоге, мы получаем:
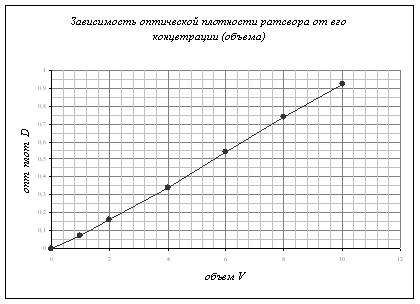 Теперь
построим калибровочную прямую, используя эти данные. Причем зависимость
оптической плотности от концентрации исследуемого раствора должна быть линейной
по закону Бугера-Ламберта-Бера
Теперь
построим калибровочную прямую, используя эти данные. Причем зависимость
оптической плотности от концентрации исследуемого раствора должна быть линейной
по закону Бугера-Ламберта-Бера ![]() , где ε – молярный
коэффициент эктсинции, l – в нашем случае - ширина
кювета, которая равна 1см.
, где ε – молярный
коэффициент эктсинции, l – в нашем случае - ширина
кювета, которая равна 1см.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.