




Федеральное агентство по образованию
Государственное образовательное учреждение высшего и профессионального образования
КРАСНОЯРСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
Кафедра «Теоретическая и общая теплотехника»
ЛАБОРАТОРНАЯ РАБОТА
Определение теплоемкости воздуха
Выполнил:
ст-т гр. НТ 84-1
И.А. Кротов
Проверил:
Г.В.Фёдоров
Красноярск 2006
1. Цели лабораторной работы а) Изучение первого закона термодинамики и теплоемкости газов.
б) Освоение методики калориметрического эксперимента на примере определения изобарной теплоемкости газов
2. Задание на работу
2.1. Усвоить теоретический материал по первому закону термодинамики и по теплоемкости, начертить схему установки и составить форму протокола для записи измерений.
2.2. Провести опыт по
измерению средней изобарной теплоемкости воздуха ![]()
![]() в интервале температур от комнатной до
30-40 0С методом проточного калориметра.
в интервале температур от комнатной до
30-40 0С методом проточного калориметра.
3.1. Составить отчет по работе, в котором привести:
а) Протокол измерений с подписью преподавателя;
б) Схему установки с марками и ценой деления шкалы приборов;
в) Обработанные результаты
опыта ( вычисление ![]() ,
, ![]() ,
, ![]() , k, u,
i, s, оценку погрешности опыта и сравнение
экспериментального значения
, k, u,
i, s, оценку погрешности опыта и сравнение
экспериментального значения ![]() с литературным).
с литературным).
3. Схема опытной установки
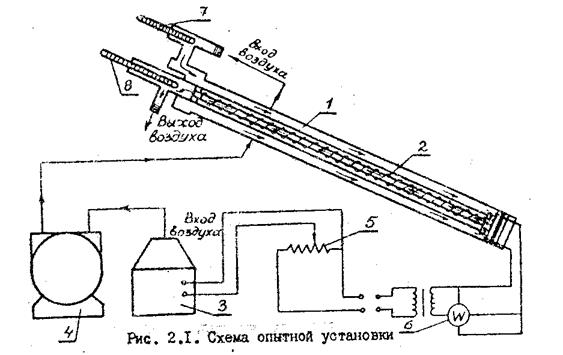
Рисунок 3.1 – Схема опытной установки
1- проточный калориметр; 2- электронагреватель; 3- электронасос; 4- газосчетчик; 5- автотрансформатор; 6- ваттметр; 7,8- ртутные термометры
4. Протокол измерений
Таблица 4.1 – Таблица измерений
|
|
W, м3 |
tвх, 0С |
tвых, 0С |
N, Вт |
Р, мм.рт.ст |
|
0 |
6,75 |
23,3 |
30,6 |
16,25 |
737 |
|
300 |
7,43 |
25 |
32 |
16,25 |
737 |
|
600 |
8,12 |
26,2 |
33,1 |
16,25 |
737 |
|
900 |
8,78 |
27,1 |
34 |
16,25 |
737 |
|
1200 |
9,46 |
27,8 |
34,4 |
16,25 |
737 |
|
1500 |
10,13 |
28 |
34,8 |
16,25 |
737 |
|
1800 |
10,81 |
28,3 |
35 |
16,25 |
737 |
5. Обработка результатов измерений
1. Определим объемный расход воздуха через калориметр
Vt=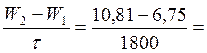 0,00225,[м3/c]
0,00225,[м3/c]
2. Рассчитываем среднюю изобарную объемную теплоемкость воздуха
![]() =
=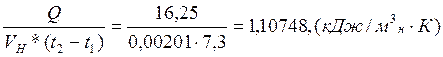
![]() Q=N , где N- мощность электронагревателя,
Вт
Q=N , где N- мощность электронагревателя,
Вт
3. Находим объемный расход воздуха VH, приведенный к нормальным условиям, из объединенного закона Бойля- Мариотта и Гей-Люссака, допустив что воздух по своим свойствам близок к идеальному газу
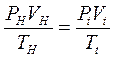
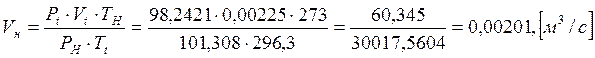
Где Tt=t1 + 273= 23,3 + 273=296,3,К
4. Вычисляем величину
расхождения между эксперементально определенной теплоемкостью ![]() и табличным значением
и табличным значением ![]()
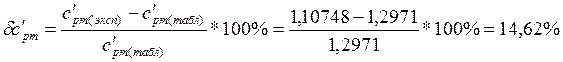
5. Для интервала температур t1-t2 найдем значение средней массовой изобарной теплоемкости
![]() =
=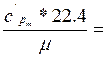
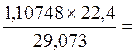 0,8533,
0,8533,![]()
Где ![]() условная молекулярная
масса воздуха, кг/к моль
условная молекулярная
масса воздуха, кг/к моль
6. Для определения изохорной массовой теплоемкости воздуха воспользуемся формулой Майера
![]() = 0,8533 – 0,287 =
0,5663,[кДж/кг*град]
= 0,8533 – 0,287 =
0,5663,[кДж/кг*град]
R=287,[Дж/кг*к]
Где R – газовая постоянная воздуха, кДж/кг*град
7. По теплоемкостям вычисляем показатель адиабаты для воздуха
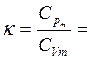
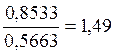
8. Рассчитываем искомые величины
![]() ,
, ![]() ,
, ![]() , k,
u, i, s
, k,
u, i, s
U= CVm*t2=0,5663*303,6=171,9,[кДж/кг]
i= CPm*t2=0,8533*303,6=259,1,[кДж/кг]
S= CPm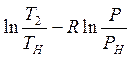 =0,8533*
=0,8533*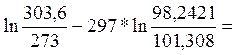 0,0906 – (-9,13)=
9,221,[кДж/кг*град]
0,0906 – (-9,13)=
9,221,[кДж/кг*град]
Вывод: 1) на опыте я ознакомился с первым законом термодинамики и теплоемкости газов;
2) освоил
методику калориметрического эксперимента, определил величину изобарной
теплоемкости газа - ![]() = 0,8533,
= 0,8533,![]() .
.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.