Пользуясь результатами измерения, построим график зависимости электропроводности от объема титранта:
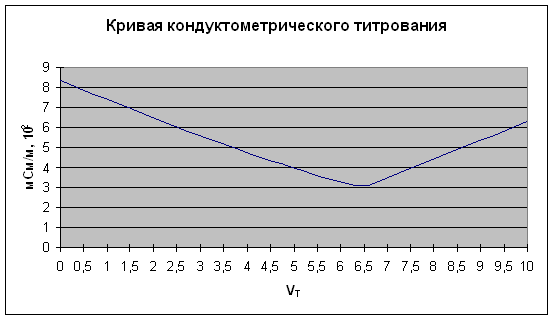
На графике получили точку эквивалентности с координатами: (6,5:3,06). Это означает, что VT = 6,5 мл. По формуле (1) находим концентрацию электролита:
![]() н.
н.
Из графика видно, что титрование проводилось сильной кислоты щелочью.
2). Определение константы диссоциации слабой кислоты (уксусная СН3СООН, 0,5н)
Таблица полученных результатов:
|
Концентрация (С), н |
Электропроводность J , мСм/м |
Температура
раствора, |
|
0,0016 |
5,9 |
20,9 |
|
0,008 |
14,23 |
20,8 |
|
0,04 |
32,60 |
20,8 |
|
0,2 |
73,15 |
20,8 |
|
1 |
148,8 |
20,8 |
По вышеприведенным
экспериментальным данным построим график зависимости: ![]() J :
J :
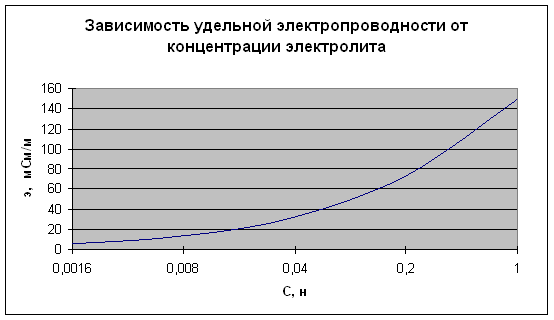
С помощью справочника физико-химических величин определяем эквивалентную электропроводность при бесконечном разведении заданной кислоты СН3СООН по формуле:
![]() .
Учитывая зависимость электропроводности от температурного коэффициента, запишем
в таблицу эквивалентные электропроводности:
.
Учитывая зависимость электропроводности от температурного коэффициента, запишем
в таблицу эквивалентные электропроводности:
|
|
|
|
Т,
|
|
366,28 |
329,42 |
36,86 |
20,9 |
|
365,68 |
328,92 |
36,76 |
20,8 |
|
365,68 |
328,92 |
36,76 |
20,8 |
|
365,68 |
328,92 |
36,76 |
20,8 |
|
365,68 |
328,92 |
36,76 |
20,8 |
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.