

Министерство образования Российской федерации
Санкт-Петербургский государственный горный институт
Отчет.
по лабораторной работе:
Исследование буферного раствора.
Группа АПМ-01
Выполнил: студент Павлов Р. Д.
Проверил: доцент Литвинова Т. Е.
дата: 25.10.02
Санкт-Петербург
2002
1. Цель работы: научиться выбирать состав буферного раствора с заданным значением рН, рассчитывать количества компонентов, необходимые для приготовления буферного раствора. Познакомиться с понятием ёмкости буферного раствора и научиться её определять. Освоить современные методы измерения водородного показателя растворов с помощью рН-метров.
2. Приборы и реактивы:
1. рН-метр;
2. мерные цилиндры объемом 100 мл и объемом 50 мл;
3. пипетка Мора объемом 5 мл;
4. мерная или коническая колба объемом 100 мл;
5. коническая колба для титрования объемом 50 мл;
6. бюретка объемом 25 мл;
7. уксусная кислота, 0,2 М раствор;
8. ацетат натрия, 0,2 М раствор;
9. гидроксид натрия, 0,2 М раствор;
10. хлорид аммония, 0,2 М раствор;
11. соляная кислота, 0,05 н раствор;
12. гидроксид натрия, 0,05 М раствор;
13. фенолфталеин;
14. метилоранж.
3. Расчет объемов исходных растворов.
По формуле
для основного буфера находим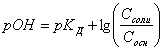 (1). Заданная
(1). Заданная ![]() и константа диссоциации
и константа диссоциации ![]() , подставив в (1), получим:
, подставив в (1), получим: 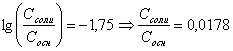 . Где
. Где ![]() и
и
![]() , тогда
, тогда ![]() .
.
![]() и
и ![]() .
Подставив эти значения, получим:
.
Подставив эти значения, получим: ![]() , т.к.
, т.к. ![]() . Следовательно
. Следовательно ![]() , а
, а ![]() .
.
4. Определение рН.
С помощью рН-метра определяем значение рН
приготовленного буферного раствора, оно равно ![]() ,
что приближенно равно заданной при расчете рН.
,
что приближенно равно заданной при расчете рН.
5. Определение емкости буфера экспериментально.
Для
определения емкости буфера экспериментально, аликвоту объемом 5 мл титруют по
кислоте (соляной) до перехода окраски метилоранжа от желтой к красной. Емкость
вычисляют по формуле: ![]() , где
, где ![]() и
и ![]() -
концентрация и эквивалентный объем титранта, а
-
концентрация и эквивалентный объем титранта, а ![]() -
аликвотный объем буферного раствора. Тогда экспериментальная емкость равна:
-
аликвотный объем буферного раствора. Тогда экспериментальная емкость равна: ![]() .
.
6. Расчет буферной емкости основного буфера по кислоте.
![]() , подставив
, подставив ![]() и
и
![]() , получим теоретическую емкость:
, получим теоретическую емкость: ![]() . Следовательно –
. Следовательно – ![]() .
.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.