За основу роботи калориметра покладено принцип диференційного розміщення двох пар однакових термобатарей. В одну з чашечок кожної пари вміщується еталонна речовина, до іншої – зразок, що досліджується. Реєструючи при лінійному нагріві корпусу тепловий потік, можливо знайти значення теплових ефектів, що супроводжують перетворення в полімерах, і температурну залежність теплоємності.
Кількість тепла, що виділяється або поглинається при перебігу хімічних перетворень можна оцінити безпосередньо з термограми:
QH = B* S (2.2 )
де B- постійна колориметра;
S- площина піка, що обмежений диференційним записом та лінією, по якій би протікала зміна ентальпії при відсутності теплового ефекту.
При визначенні постійної В як еталонної речовини використовували бензойну кислоту, що атестована по величині теплоти плавлення.
При дослідженні кінетичних закономірностей тужавіння по тепловиділенню наважку зразка, що досліджується, брали у кількості 0,150 ± ± 0,015. 10-3 кг. Як зразок використовували модельні ЕФУ та композиції на основі ЕФУ з акриловою, пропіоновою, каприловою, ліноленовою кислотами.
3) Твердість плівок визначали на маятниковому приладі МА-3 за ГОСТ 5233-89. Дослідження процесу тужавіння проводили в тонких плівках. Перед тужавінням плівкотвірної речовини, що нанесена методом наливу, її витримували на повітрі протягом 10 хв. під кутом 45° (для отримання плівок товщиною 25±5 мкм). Тужавіння плівок здійснювали в термостаті при заданій температурі.
4) Вміст тривимірної сітки в полімері визначали методом золь - гель - фракції. Метод визначення ступеню тужавіння плівок за вмістом золь - гель - фракції заснований на здатності розчинної частини плівки (золь-фракції), не пов’язаної з полімерною сіткою (гель-фракцією), вимиватися органічним розчинником.
Метод пов’язаний з кількісним визначенням золь-фракції за допомогою екстрактора Сокслета, що працює в автономному режимі.
Вміст золь-фракції Z (%) визначають за формулою (3.3) :
Z = ( G0 – Gn ) . 100 /a , (2.3)
Де G0 – Gn – маса патрону з наважкою лакової плівки до та після екстрагування протягом n- годин;
а – наважка плівки, г [23 ].
5) Стійкість покриття до дії ударних згинаючих навантажень визначали у відповідності за ГОСТ 15140-78.
6) Ступінь висихання покриття визначали у відповідності з ГОСТ 19007-78.
2.2 Практична частина
2.2.1 Дослідження кінетики реакцій взаємодії ЕФУ з карбоновими кислотами.
Зразки готувалися із розрахунку мольного співвідношення ЕФУ до обраної кислоти 1:1, а також із додаванням вищевказаного каталізатора з концентрацією 1% і 2% (мас.).
Зразки витримували в термостаті з температурою +100 ºС. Винятком був зразок ЕФУ з акриловою кислотою, який витримувався при температурі +50 ºС для запобігання можливій реакції полімеризації кислоти.
Через певні проміжки часу проводили вимірювання К. Ч. кожного зразка. В результаті цього отримали графічні залежності К. Ч. = f (t), які наведені нижче.
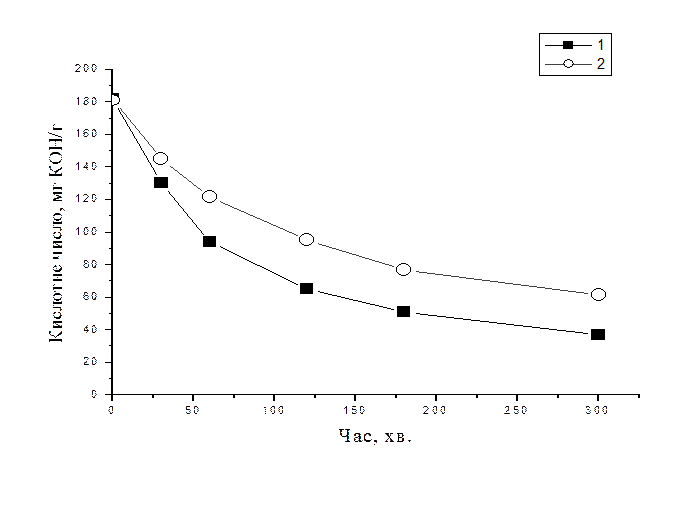
Рис. 2.2.1 Зміна кислотного числа реакційної суміші ЕФУ + АК при різних
концентраціях каталізатора: 1) 2 % (мас.); 2) 1 % (мас.)
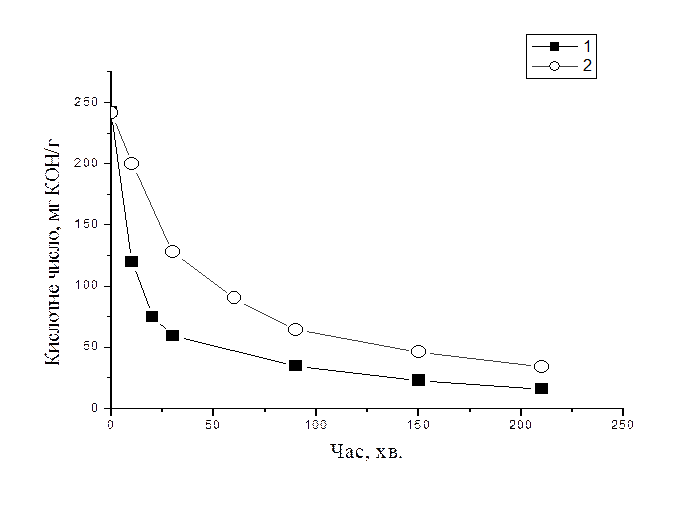
Рис. 2.2.2 Зміна кислотного числа реакційної суміші ЕФУ + ПК при різних
концентраціях каталізатора: 1) 2 % (мас.); 2) 1 % (мас.)
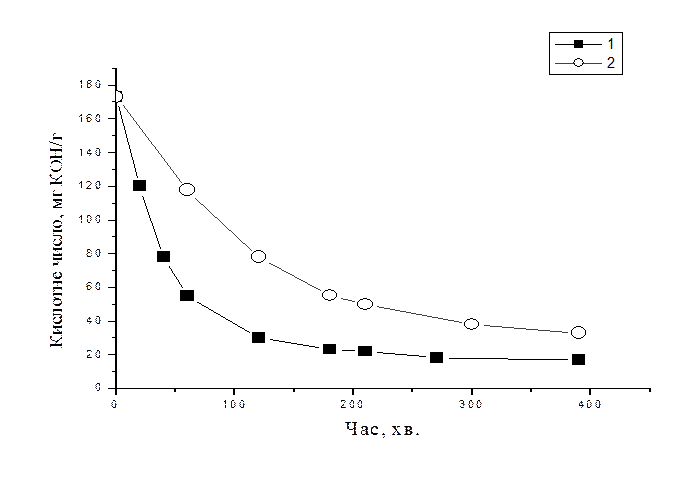
Рис. 2.2.3 Зміна кислотного числа реакційної суміші ЕФУ + КК при різних
концентраціях каталізатора: 1) 2 % (мас.); 2) 1 % (мас.)
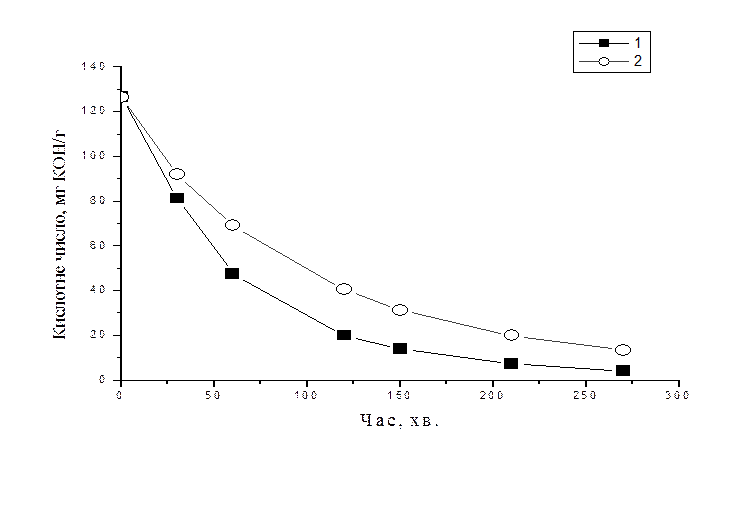
Рис. 2.2.4 Зміна кислотного числа реакційної суміші ЕФУ + ЛК при різних
концентраціях каталізатора: 1) 2 % (мас.); 2) 1 % (мас.)
Одночасно проводили розрахунок ступенів завершеності реакції при кожному значенні К. Ч. За вищенаведеним алгоритмом визначали константи швидкості реакцій. Отримані дані зведені до таблиці 2.2.
Таблиця 2.2 – Кінетичні характеристики реакцій ЕФУ з карбоновими
кислотами (1:1)
|
Реакційна суміш, температура реакції |
Концентрація каталізатора, % (мас.) |
Порядок реакції |
Константа швидкості реакції, хв.-1 ∙ 10 2 |
|
Ліноленова к-та + + ЕФУ, 100 ºС |
1 |
І |
0,84 |
|
2 |
1,3 |
||
|
Каприлова к-та + + ЕФУ, 100 ºС |
1 |
ІІ |
1,17 |
|
2 |
3,3 |
||
|
Акрилова к-та + + ЕФУ , 50 ºС |
1 |
ІІ |
0,66 |
|
2 |
1,3 |
||
|
Пропіонова к-та + + ЕФУ, 100 ºС |
1 |
ІІ |
2,83 |
|
2 |
6,3 |
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.