







Министерство здравоохранения Республики Беларусь
Учреждение образования
«Гомельский государственный медицинский университет»
Кафедра общей и биоорганической химии
Обсуждено на заседании кафедры ___________________
Протокол №_____________________________________
МЕТОДИЧЕСКАЯ РАЗРАБОТКА
для проведения занятия со студентами I курса
лечебного факультета по биоорганической химии
Тема № 6: Реакции элиминирования и нуклеофильного
замещения у насыщенного атома углерода
Время: 3 часа
1. УЧЕБНЫЕ И ВОСПИТАТЕЛЬНЫЕ ЦЕЛИ:
Сформировать знания о конкурентных реакциях SN и Е, протекающих в одной молекуле, но на разных реакционных центрах. Выработать у студентов умение прогнозировать реакционную способность спиртов, аминов, тиолов и галогенпроизводных углеводородов в конкурентных реакциях нуклеофильного замещения и элиминирования в зависимости от строения субстрата и типа реагента.
МОТИВАЦИЯ ДЛЯ УСВОЕНИЯ ТЕМЫ:
Конкурентные реакции SN и Е широко представлены в биологических системах, а также лежат в основе многочисленных промышленных синтезов.
ТРЕБОВАНИЯ К ИСХОДНОМУ УРОВНЮ ЗНАНИЙ:
а) электроотрицательность элементов;
б) электронные эффекты заместителей. Электронодонорные и электроноакцепторные заместители;
в) полярность и поляризуемость связей;
г) типы реагентов (нуклеофил). Переходное состояние. Строение карбкатиона и карбаниона. Факторы, влияющие на их стабильность;
д) кислотность и основность органических соединений.
В результате проведения занятия студент должен:
1) знать:
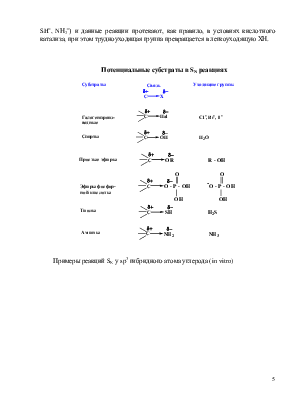
- реакционные центры в молекуле у sp3-гибридного атома углерода, связанного с электроакцепторным заместителем;
- механизм конкурентных реакций нуклеофильного замещения и элиминирования;
- биологические реакции (алкилирование и дегидратация), протекающие по типу SN и Е
2) уметь:
- находить реакционные центры у насыщенного атома углерода, связанного с электроакцепторным заместителем в молекулах органических соединений;
- описывать механизмы реакций SN и Е, протекающие в биологических системах.
2. СВЯЗЬ СО СМЕЖНЫМИ ДИСЦИПЛИНАМИ:
Полученные знания о конкурентных реакциях, протекающих в одной молекуле, но на разных реакционных центрах потребуются студентам при изучении курсов биохимии, фармакологии.
3. КОНТРОЛЬНЫЕ ВОПРОСЫ ПО ТЕМЕ ЗАНЯТИЯ:
3.1 Реакции нуклеофильного замещения в ряду алкилгалогенидов, спиртов, тиолов, аминов.
3.2 Реакции β-элиминирования как наиболее распространенный тип элиминирования, протекающий в живых организмах и приводящий к образованию кратной связи.
4. ХОД ЗАНЯТИЯ:
4.1. Реакции нуклеофильного замещения (SN)
К конкурентным реакциям у насыщенного атома углерода относятся реакции нуклеофильного замещения и элиминирования.
Конкурентные реакции SN и Е протекают в одной молекуле, но на разных реакционных центрах. Они протекают с участием нуклеофила у sp3-гибридного атома углерода, связанного полярной связью (σ-связью) с заместителем.
Нуклеофильное замещение при насыщенном атоме углерода характерно для алкилгалогенидов, спиртов, тиолов, аминов.
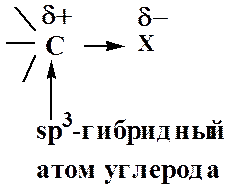
Введение в насыщенный углеводородный скелет молекулы электроакцепторной группировки Х приводит к перераспределению электронной плотности в молекуле и появлению новых реакционных центров.
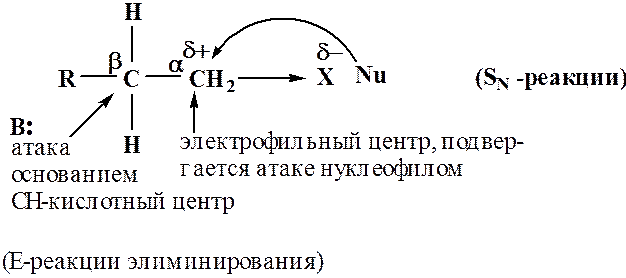

В продукте реакции новая связь образуется за счет электронной пары, которую приносит нуклеофил, а к уходящей группе переходят электроны бывшей связи С–Х.
Реакция возможна, т.е. протекает вправо, когда уходящая группа более стабильна, чем нуклеофил, т.е. имеет меньшую энергию по сравнению с атакующим нуклеофилом.
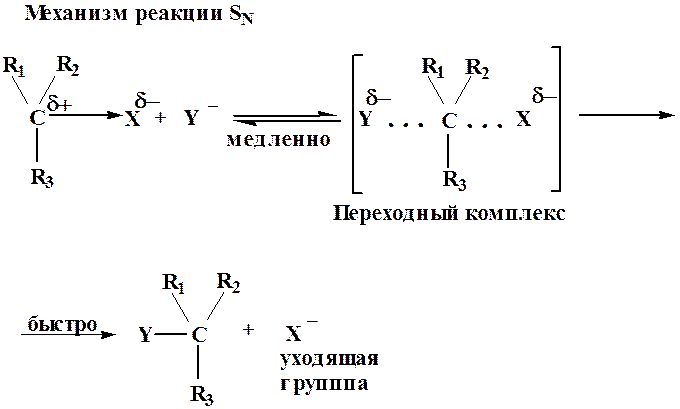
Образование молочной кислоты, протекающей по механизму SN.
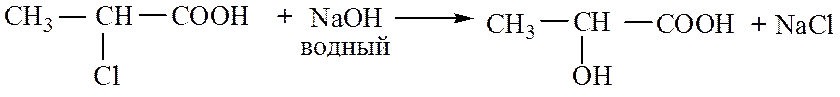
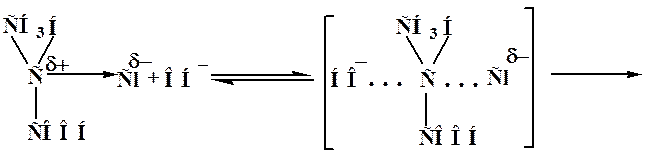
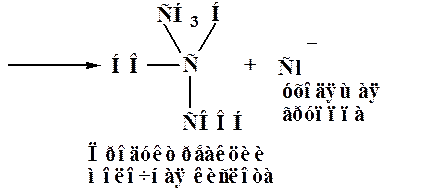
Вначале нуклеофильная частица Y‾ атакует атом углерода с наиболее выгодной стороны (противоположной уходящей группе «атака с тыла»). Разрыв старой связи С–Х и образование новой С–Y происходит синхронно, т.е. образуется переходное состояние (в этой стадии принимают участие две молекулы – реагент и субстрат). Реакция бимолекулярная, скорость реакции зависит от концентрации обоих реагентов. Переходное состояние соответствует максимуму на энергетической кривой.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.