







Последовательный ряд элементов, размещённый в порядке убывания заряда ядра атомов
3. Последовательный ряд элементов, размещённый в порядке возрастания числа электронов на последнем уровне элементов
4. Последовательный ряд элементов, размещённый в порядке убывания числа электронов на последнем уровне элементов
5. Ответы 1 и 3
Атомная масса какого химического элемента периодической системы Менделеева равна единице
1. Гелий 2. Углерод 3. Водород 4. Азот 5. Кислород
1. Максимальное число электронов во внешних подоболочках 2. Атомная масса химического элемента
3. Заряд ядра химического элемента 4. Наивысшая проявляемая валентность химического элемента
5. Ответы 1 и 4
Какая из электронных формул является электронной формулой атома Na
1. ![]() 2.
2. ![]() 3.
3. ![]()
4. ![]() 5.
5. ![]()
Название какого химического элемента обозначается: Cu
1. Кальций 2. Хлор 3. Медь 4. Хром 5. Бром
Какой принцип лежит в основе систематики заполнения электронных состояний в атомах, позволяющий объяснить периодическую систему Менделеева
1. Принцип Менделеева 2. Принцип Паули 3. Принцип Вернадского
4. Принцип Дальтона 5. Принцип Бутлерова
Какой из элементов имеет
такую электронную формулу: ![]()
1. O 2. F 3. Ne 4. Ni 5. C
Элементы, в атомах которых s- и p- состояния наружной оболочки заполнены и ими завершаются очередные периоды Периодической системы:
1. Химически инертны 2. Химически активны 3. Радиоактивны
4. Изотропны 5. Анизотропны
Что обозначают буквы K, L, M, N в Периодической системе
1. Порядковые номера элементов 2. Периоды 3. Электронные оболочки
4. Подоболочки 5. Ничего не обозначают
Начальные элементы периодов, у которых последний электрон находится в s – состоянии являются:
1. Щелочноземельные металлы 2. Щелочные металлы 3. Чёрные металлы
4. Цветные металлы 5. Ответы 1 и 2
Кем была открыта периодичность в химических свойствах элементов, которая объясняется повторяемостью в структуре внешних оболочек у атомов родственных элементов
1. Менделеевым 2. Паули 3. Бутлеровым
![]() 4.
Марковниковым 5. Дальтоном
4.
Марковниковым 5. Дальтоном
Чем описывается идеальный газ из бозонов – бозе-газ?
1. квантовой статистикой Бозе-Эйнштейна 2. квантовой статистикой Ферми-Дирака
3. квантовой статистикой Максвелла-Больцмана 4. квантовой статистикой Бозе
5. квантовой статистикой Эйнштейна
Укажите формулу распределения Бозе-Эйнштейна.
1. 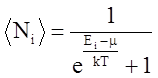 2.
2. 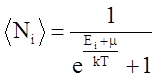 3.
3.
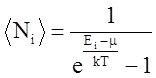
4. 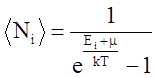 5.
5. 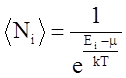
Чем является формула 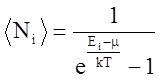 ?
?
1. Распределением Бозе-Эйнштейна 2. Распределением Максвелла
3. Распределением Больцмана 4. Распределением Ферми-Дирака
5. Распределением Эйнштейна
Чем является ![]() в формуле
в формуле 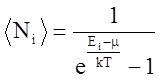 ?
?
1. среднее число бозонов 2. электрохимический потенциал
3. химический потенциал 4. параметр вырождения
Химический потенциал ![]() в формуле
в формуле
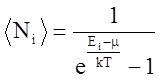 должен быть:
должен быть:
1. ![]() 2.
2. ![]() 3.
3.
![]() 4.
4.
![]() 5.
5.
![]() =0
=0
Идеальный газ из фермионов – ферми-газ описывается:
1. квантовой статистикой Бозе-Эйнштейна 2. квантовой статистикой Ферми
3. квантовой статистикой Максвелла-Больцмана 4. квантовой статистикой Дирака
5. квантовой статистикой Ферми-Дирака
1. 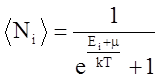 2.
2. 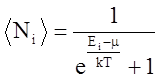 3.
3.
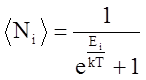
4. 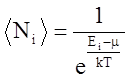 5.
5.
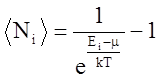
Химический потенциал ![]() в
формуле
в
формуле 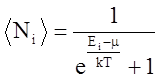 может быть:
может быть:
1. только ![]() 2.
только
2.
только ![]() 3.
3. ![]() =0
=0
4. как![]() так и
так и ![]() 5.
5. ![]() >0
>0
Формула 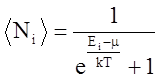 является:
является:
1. Распределением Бозе-Эйнштейна 2. Распределением Максвелла-Больцмана
3. Распределением Больцмана 4. Распределением Эйнштейна
5. Распределением Ферми-Дирака
Формула 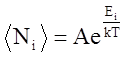 - это:
- это:
1. Распределением Бозе-Эйнштейна 2. Распределением Ферми
3. Распределением Максвелла-Больцмана 4. Распределением Дирака
5. Распределением Ферми-Дирака
При каком условии распределения Бозе-Эйнштейна и Ферми-Дирака переходят в распределение Максвелла-Больцмана?
1. А<<1
2. 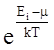 >>1 3. A>>1 4.
в 1 и 2 случаях 5.
>>1 3. A>>1 4.
в 1 и 2 случаях 5. 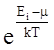 <<1
<<1
Чем является А в формуле 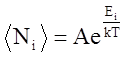 ?
?
1. параметр вырождения 2. химический потенциал
3. температура вырождения 4. число заполнения
Температурой вырождения ![]() называется
температура:
называется
температура:
1. при которой отчётливо проявляются квантовые свойства идеального газа, обусловленные тождественностью частиц
2. выше которой отчётливо проявляются квантовые свойства идеального газа, обусловленные тождественностью частиц
3. ниже которой отчётливо проявляются квантовые свойства идеального газа, обусловленные тождественностью частиц
4. ниже которой квантовые свойства идеального газа не проявляются
5. при которой квантовые свойства идеального газа не проявляются
![]() Узкий пучок атомов водорода, заведомо
находящийся в S-состоянии, в неоднородном
магнитном поле расщепляется на:
Узкий пучок атомов водорода, заведомо
находящийся в S-состоянии, в неоднородном
магнитном поле расщепляется на:
1. три пучка 2. четыре пучка 3. два пучка 4. один пучок 5. на 10n пучков
Магнитный момент атома связанный с орбитальным движением электрона, пропорционален:
1. кинетическому моменту 2. статическому моменту 3. механическому моменту
4. гироскопическому моменту 5. дипольному моменту
Для объяснения тонкой структуры спектральных линий, а также ряда других трудностей в атомной физике американские физики Д. Уленбек (1900 — 1974) и С. Гаудсмит (1902 — 1979) предположили, что электрон обладает:
1. собственным механическим моментом импульса
2. собственным неуничтожимым статическим моментом импульса
3. собственным неуничтожимым механическим моментом импульса
4. собственным неуничтожимым моментом импульса
Согласно общим выводам квантовой механики, спин квантуется по закону:
1.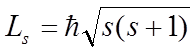 2.
2. 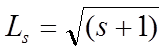 3.
3. 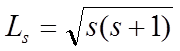
4. 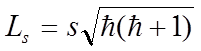 5.
5. 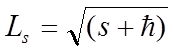
В формуле 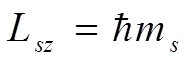 ,
ms :
,
ms :
1. спиновое квантовое число 2. магнитное спиновое квантовое число
![]() 3. собственный неуничтожимый механический момент импульса 4. масса точки S
3. собственный неуничтожимый механический момент импульса 4. масса точки S
Самый нижний уровень Е1, отвечающий минимальной возможной энергии, называется
1. Первый 2. Основной 3. Главный
4. Возбужденный 5. Минимальный
По мере роста главного квантового числа n энергетические уровни располагаются
1. теснее 2. свободнее
3. их расположение не зависит от главного квантового числа
4. их расположение зависит от того четное оно или нечетное
При каких Е движение электрона является свободным
1. При Е<0 2. При Е=0</A> 3. При Е>0</A>
4. Электрон всегда движется свободно
5. Электрон не при каких условиях не может двигаться свободно
Момент импульса (механический орбитальный момент) электрона квантуется - это значит, что
1. принимает значения 0,1,2,… т.е. любые целые положительные числа и ноль
2. принимает значения 1,2,… т.е. любые целые положительные числа
3. принимает конкретные значения которые определяются формулой 1
4. т.е. не имеет точного значения в данный момент времени
5. принимает конкретные значения которые определяются формулой 2
Эффекта Зеемана это:
1. Расщепление уровней энергии во внешнем электрическом поле
2. расщепление энергетических уровней в магнитном поле
3. явление нахождения атома в нескольких различных состояниях при
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.