
Министерство образования Российской Федерации
Санкт-Петербургский государственный горный институт им. Г.В. Плеханова
(технический университет)

кафедра геоэкологии
Выполнил: студентка гр. ЭГ-03 ____________ /Шульгина Е.Д./
(подпись) (Ф.И.О.)
ОЦЕНКА: _____________
Дата: __________________
(должность) (подпись) (Ф.И.О.)
Санкт-Петербург
2004
Цель работы - Фотометрическое определение концентрации вещества по измеренному значению оптической плотности при помощи комбинированного графика, построенного по серии точек стационарного раствора.
Приборы и реактивы: - фотоколориметр КФК-3
- мерные колбы ёмкостью 50 мл - 7 шт.
- пипетки градуированные на 1 и 10 мл
- стандартный раствор соли Fe 0,1 г/л
- азотная кислота, разбавленная 1:1
- Родонит аммония (или К), 10-типроцентный раствор
- рабочий раствор соли Fe 0,8 ммоль/л
- задача с исследуемым раствором с концентрацией по железу
18-30 мг/л
|
№ |
V р-р. (мл) |
CFe (мг/л) (в 50 мл) |
D |
|
1 |
0 |
0 |
0,000 |
|
2 |
1 |
0,9 |
0,134 |
|
3 |
2 |
1,8 |
0,243 |
|
4 |
4 |
3,6 |
0,539 |
|
5 |
6 |
5,4 |
0,782 |
|
6 |
8 |
7,2 |
1,052 |
|
7 |
10 |
9,0 |
1,302 |
|
З |
5 |
0,685 |
Задача:
Колибровочный график
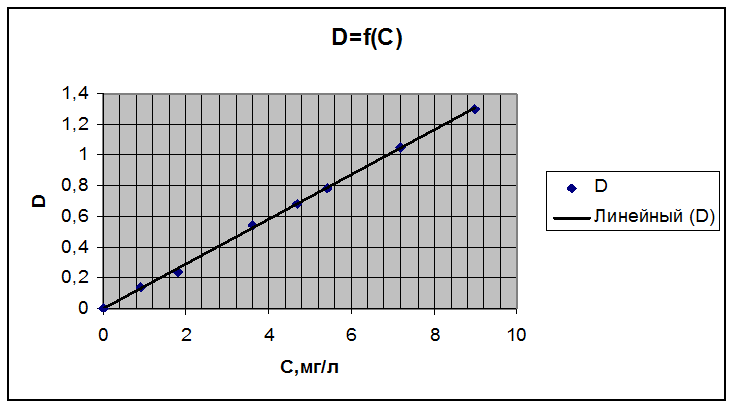
Из данного графика следует, что при оптической плотности D = 0,685 концентрация железа CFe = 4,7 мг/л.
Cист = C3 * 10 = 4,7*10 = 47 мг/л
Вывод: При помощи фотометрического метода определения концентрации железа CFe по измеренному значению оптической плотности D фотоколориметром КФК - 3 был построен колибровочный график. При известной оптической плотности раствора задачи D = 0,685 определили концентрацию железа CFe = 4,7 мг/л. Так как раствор задачи был разбавлен в 10 раз, то Cист = C3 * 10 = 47 мг/л
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.