1. Аналитический и практический расчета энергии активации.
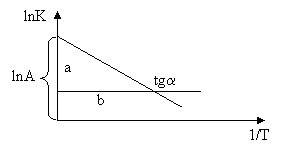 Графический
способ.
Графический
способ.путем логарифмирования
K=A*e–Ea/RT
K – константа скорости
A – предэкспонентационный множитель
lnK=lnA-{(Ea/R)*(1/T)}
KT1= A*e–Ea/RT1
A – учитывая стерический фактор (пространственное расположение молекул). (Учитывается строение молекулы, с какой стороны пойдет молекула).
KT2= A*e–Ea/RT2
KT2/ KT1= e(Ea/R)(1/T1-1/T2)
ln KT2/ KT1=(Ea/R)(1/T1-1/T2)
При двух температурах, зная значение двух констант скоростей, можно рассчитывать энергию активации.
Если реакция идет на поверхности раздела фаз, то величину константы равновесия подставляют только в величину парциального давления газа (поглощение CO2 углем).
ln KP2/ KP1=(Ea/R)(1/T1-1/T2)
2. Способы защиты металла от коррозии
1. Электрохимический способ
1) протекторная (анодная)
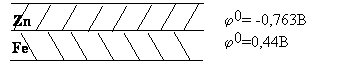 |
2) катодная
от внешнего источника тока на металл дают положительный потенцил, а в качестве анода используют любой металлический лом.
2. Металлические покрытия
1) анодные
|
||||
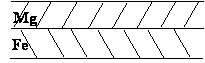 |
||||
2) катодные
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.