Для кристалла нитрата висмута-эрбия-лантана с концентрацией раствора 0,60 г/мл при t = 15 ْС – для размера кристалла в продольном направлении полученные статистические данные:
|
Коэффициент корреляции rxy |
0,952397358 |
|
Коэффициент детерминации R2 |
0,907060728 |
|
Критерий значимости Фишера F |
6,25856 *10-15 |
|
Уравнение регрессии |
|
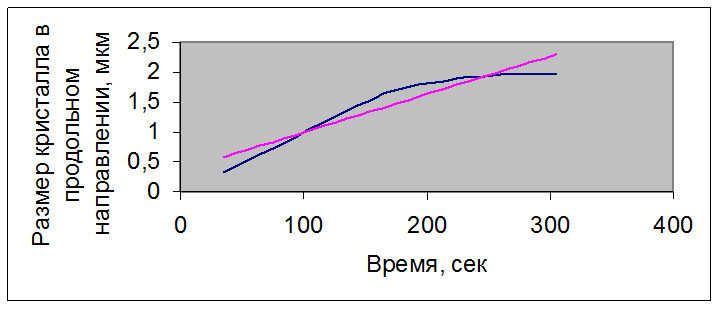
Рисунок 3.54 – Зависимость размера кристалла нитрата висмута-эрбия-лантана с концентрацией раствора 0,60 г/мл от времени при t =15 ºС
Для кристалла нитрата висмута-эрбия-лантана с концентрацией раствора 0,60 г/мл при t = 35 ْС – для размера кристалла в продольном направлении полученные статистические данные:
|
Коэффициент корреляции rxy |
0,990439534 |
|
Коэффициент детерминации R2 |
0,98097047 |
|
Критерий значимости Фишера F |
4,95838 *10-23 |
|
Уравнение регрессии |
|
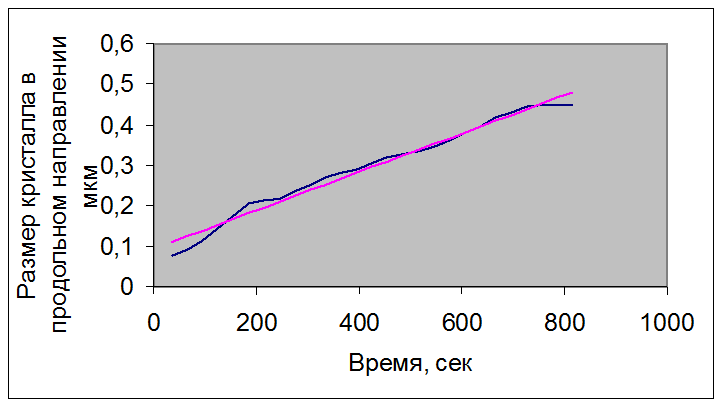
Рисунок 3.55 – Зависимость размера кристалла нитрата висмута-эрбия-лантана с концентрацией раствора 0,60 г/мл от времени при t =35 ºС
После кристаллизации проводили термическую обработку полученных кристаллов с целью синтеза ионопроводящих фаз. Выбор температуры синтеза осуществляли по данным дифференциально-термического анализа.
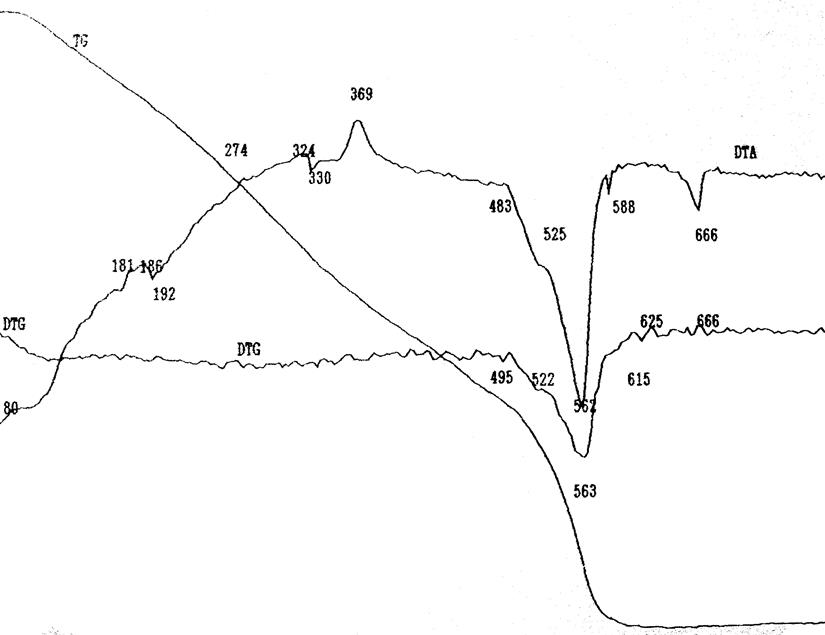
Рисунок 3.56 – Дериватограмма образца Bi8Er2O15
Из приведенных данных на рисунке 12 видно, что имеется несколько экзотермических эффектов в интервале температур 180–370ºС, которые, вероятно, соответствуют разложению гидроксидов, что подтверждается потерями массы. Эндотермический пик соответствует началу фазообразования в исследуемых системах. Фазообразование начинается при температуре ≈ 490 ºС, что значительно ниже температур, необходимых на стадии отжига при твердофазном синтезе.
Данные ДТА образца Bi(NO3)3 – Er(NO3)3 – La(NO3)3 приведены на рисунке 3.57.
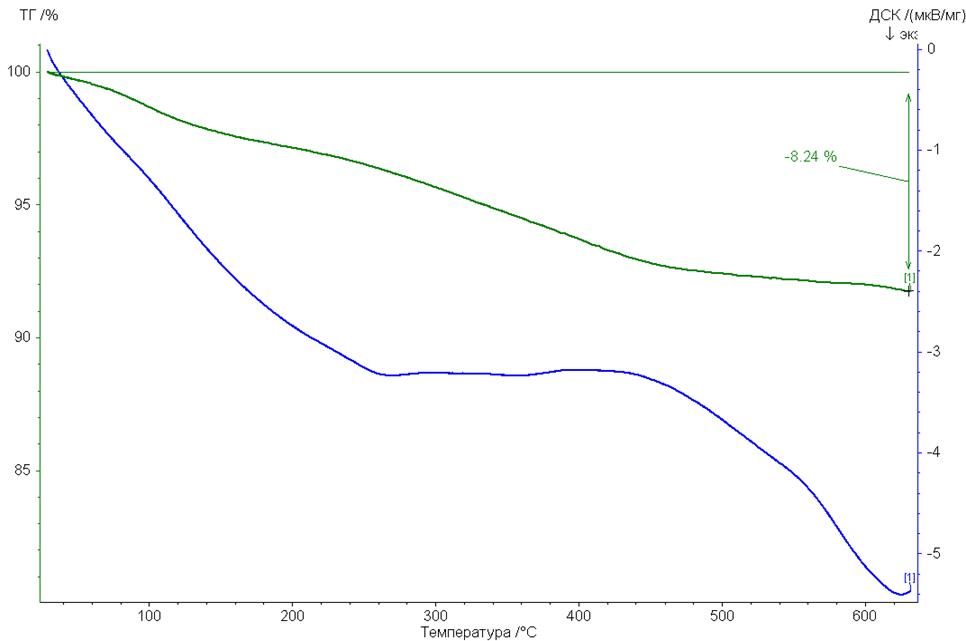
Рисунок 3.57 – Дериватограмма образца Bi(NO3)3 – Er(NO3)3 – La(NO3)3
Из приведенных данных следует, что фазообразование в системе начинается при температуре 440 ºС, при температуре 620 ºС тепловой эффект данного процесса достигает своего максимального значения. В связи с этим синтез фаз целесообразно проводить в интервале температур ~ 600-620 ºС.
На рисунках 3.58-3.63 приведены данные РФА, в таблице – 3.19 представлены данные по составам синтезированных образцов.
Таблица 3.19 – Состав синтезированных образцов
|
№ образца |
Исходные мольные соотношения оксидов |
Метод синтеза |
Температура обработки, ºС |
Состав образца по данным РФА |
|
1 |
8 Bi2O3 – 2 Er2O3 |
Совместное растворение оксидов |
300 |
Er2O3 – 20,8 % Bi(OH)3 – 79,2 % |
|
2 |
8 Bi2O3 – 2 Er2O3 |
Совместное растворение оксидов |
600 |
Bi8Er2O15 – 100 % |
|
3 |
8 Bi2O3 – 2 Er2O3 |
Соосаждение гидроксидов |
300 |
Er2O3 – 5,2 % Bi(OH)3 – 94,1 % Bi2O3 – 0,7 % |
|
4 |
8 Bi2O3 – 2 Er2O3 |
Соосаждение гидроксидов |
600 |
Bi7,5Er2,5O15 – 83 % Bi2O3 – 17 % |
|
5 |
8 Bi2O3 – 1,8 Er2O3 – 0,2 La2O3 |
Cоосаждение гидроксидов |
300 |
Bi2O3 – 82,8 % Er2O3 – 2,44 % La2O3 – 0,16 % Bi(OH)3 – 14,6 % |
|
6 |
8 Bi2O3 – 1,8 Er2O3 – 0,2 La2O3 |
Соосаждение гидроксидов |
600 |
Er2O3 – 7 % Bi8,24La1,76O15 – 27 % Bi5.1Er4.9O15 – 66 % |
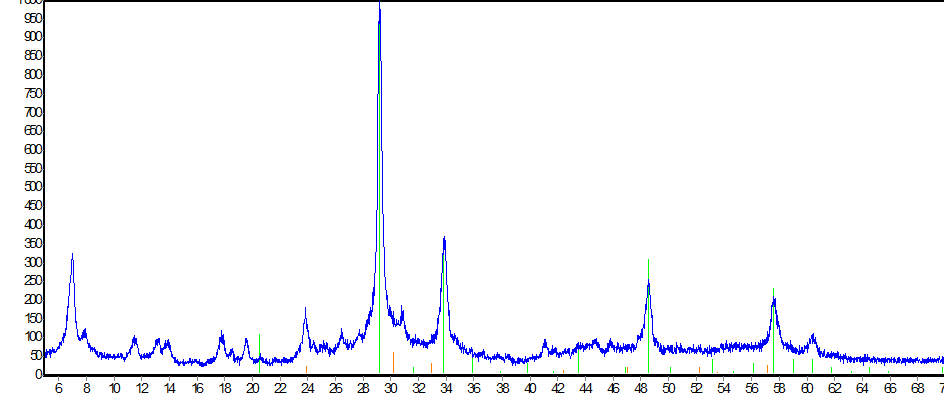
Рисунок 3.58 – Рентгенограмма образца Bi2O3 – Er2O3, полученного совместным растворением оксидов, после осушения при 300°С
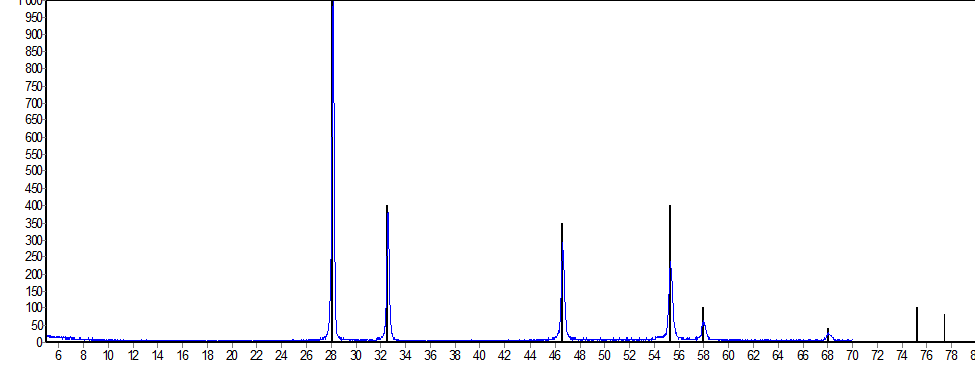
Рисунок 3.59 – Рентгенограмма образца Bi2O3 – Er2O3, полученного совместным растворением оксидов, после отжига при 600°С
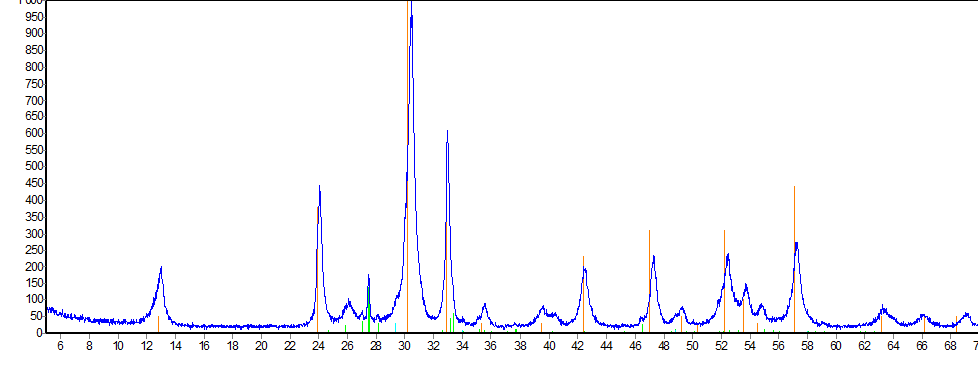
Рисунок 3.60 – Рентгенограмма образца Bi2O3 – Er2O3, полученного химическим соосаждением, после осушения при 300°С
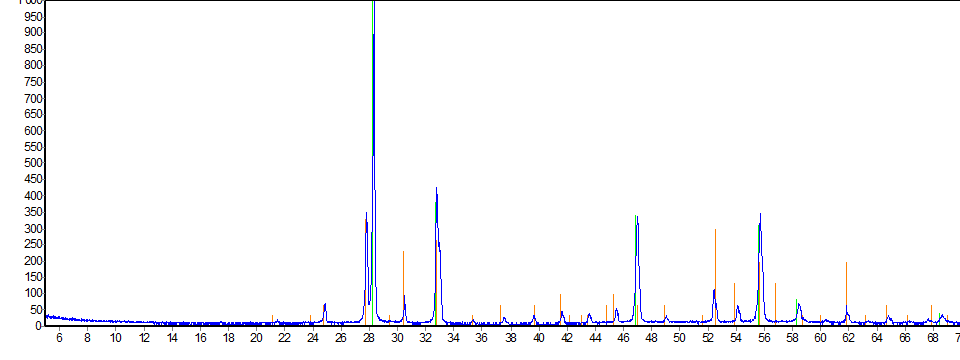
Рисунок 3.61 – Рентгенограмма образца Bi2O3 – Er2O3, полученного химическим соосаждением, после отжига при 600°С
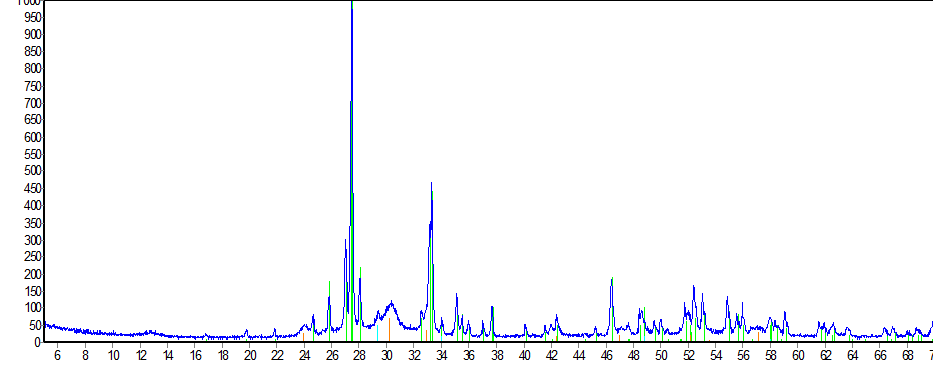
Рисунок 3.62 – Рентгенограмма образца Bi2O3 – Er2O3 – La2O3 после осушения при 300°С
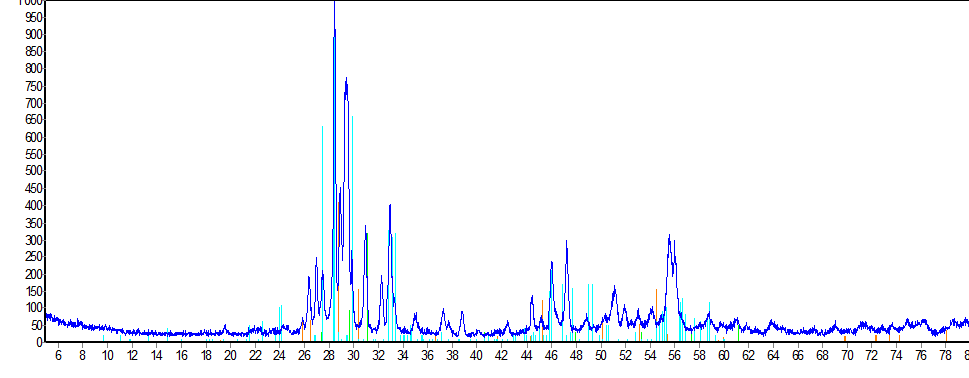
Рисунок 3.63 – Рентгенограмма образца Bi2O3 – Er2O3 – La2O3 после отжига при 600°С
На рентгенограммах образцов системы Bi2O3 – Er2O3, полученных совместным растворением оксидов и соосаждением оксидов, при температуре 300 ºС преимущественно образуется Bi(OH)3, а также остаются не вступившие в реакцию оксиды висмута и эрбия. В результате термической обработки при 600 ºС в течении одного часа в системе, полученной при совместном растворении оксидов висмута и эрбия, образуется фаза Bi8Er2O15, в системе, полученной при совместном осаждении оксидов висмута и эрбия, преимущественно формируется фаза Bi7,5Er2,5O15, а также остается не прореагировавший оксид висмута, вероятно, требуется более продолжительная термическая обработка для получения ионопроводящей фазы.
На рентгенограммах образца c содержанием оксида лантана 10 мол % при температуре 300 ºС преимущественно образуется Bi(OH)3, при 600 ºС образуются Bi5,1Er4,9O15 и Bi8,24La1,76O15, а также остается Er2O3, для получения однофазного образца необходимо проводить более длительный синтез, либо при температуре ~ 620 ºС.

Рисунок 3.64 – Кристаллы образца системы Bi2O3 – Er2O3, полученного совместным растворением оксидов, после отжига при 600 ºС
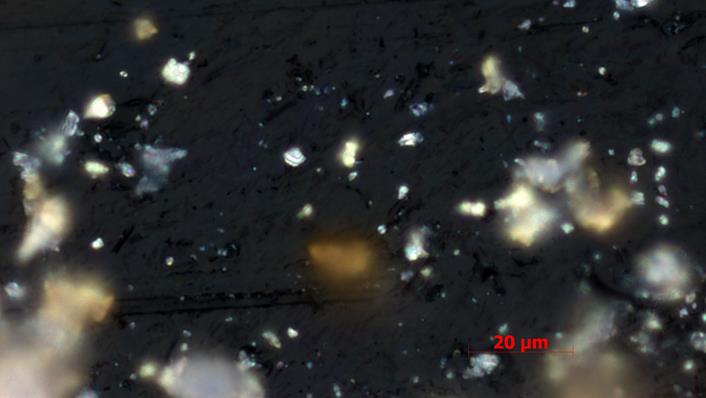
Рисунок 3.65 – Кристаллы образца системы Bi2O3 – Er2O3, полученного химическим соосаждением, после отжига при 600 ºС


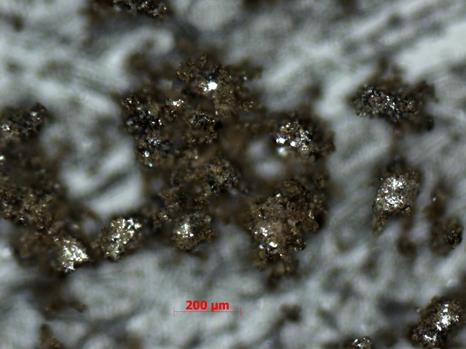
Рисунок 3.66 – Кристаллы образца системы Bi2O3 – Er2O3 – La2O3 после отжига при 600 ºС
Структура кристаллов системы Bi2O3 – Er2O3 и Bi2O3 – Er2O3 – La2O3, полученных при нарушении технологии, выглядит совершенно иначе, чем на представленных рисунках 3.1 – 3.48. Полученные в нашей работе кристаллы «оксидов», имеющие форму дендритов представлены на рисунках 3.67 – 3.68. Это говорит о том, что сформировался твёрдый раствор на основе двойного оксида висмута-эрбия, имеющий различный сосав в ветвях дендритов. аналогичные формирования твёрдых растворов происходят в металлических сплавах.


Рисунок 3.67 – Кристаллы системы Bi2O3 – Er2O3, полученные при нарушении технологии

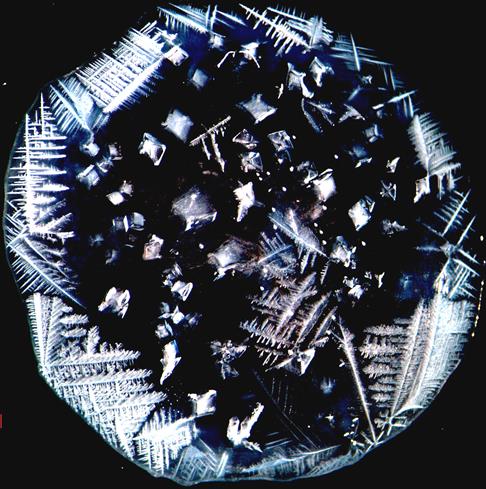
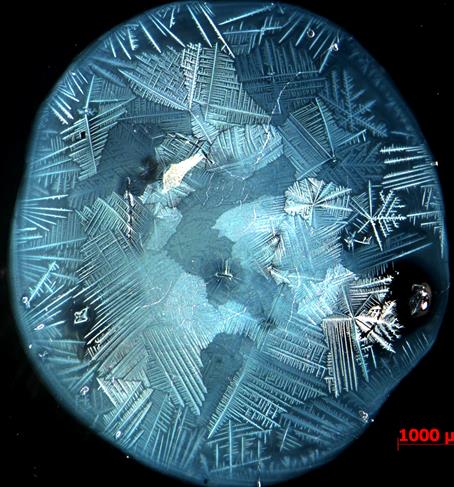
Рисунок 3.68 – Кристаллы системы Bi2O3 – Er2O3, полученные при нарушении технологии
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.