2. Определяем кратность газа m из уравнения теплового баланса для газоводяного подогревателя 4, в котором процесс 4-5 нагрева питательной воды до состояния кипения осуществляется за счет теплоты отработавших газов газового цикла (процесс b-c):
![]() m
m![]() =
= ![]() m =
m = ![]()
3.
Удельная полезная работу (![]() ) пароводяного
цикла:
) пароводяного
цикла: ![]() =
= ![]()
4.
Теоретическое удельное количество теплоты (![]() ), полученное
рабочим телом:
), полученное
рабочим телом:
![]() =
= ![]()
5.
Определим теоретический к.п.д. парогазового цикла. ![]() =
= ![]()
Для пароводяного цикла ![]() = 1 – T1/T2
= 1 – T1/T2
6. Определим термический к.п.д. парогазового цикла.
![]()
![]() ;
; ![]() =
= ![]() +
+ ![]() ;
; ![]() =
= ![]() +
+ ![]() ;
; ![]() =
= ![]() ;
; ![]() =
= ![]() =
= ![]()
Вариант 12
I. Расчет газового цикла:
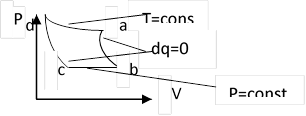
1). Определим параметры рабочего тела (р, υ, T) для основных точек цикла.
 |
Определяем газовую постоянную смеси,
![]() =
= ![]() ; R=
; R= ![]() ; где k=8314,2,
; где k=8314,2, ![]()
![]() =
= ![]() = 138,57
= 138,57 ![]()
![]() =
= ![]() = 319,78
= 319,78 ![]()
![]() =
= ![]() = 461,9
= 461,9 ![]()
![]() =
= ![]() = 259,8
= 259,8 ![]()
rCO 2 = 0,16; rCO 2 = 0,75; rCO 2 = 0,05; rCO 2 = 0,04
![]() = 1 / ((0,16/189)
+ (0,75/292,75) + (0,05/461,9) + (0,04/259,82)) =
= 1 / ((0,16/189)
+ (0,75/292,75) + (0,05/461,9) + (0,04/259,82)) =
= 272,04 ![]()
Точка a:
Pa = 6*105 Па
ta = td = 149,2 oC = 422,35 K
υa = (Rсм/Ta)/Pa = (272,04/422,35)/6*105 = 0,1912 м3/кг
Точка b:
Рb = Рс = 4*105 Па
υb = υa/(Pb/Рa)1/k = 0,191/(4*105/6*105) = 0,26 м3/кг
tb = (Pb* υb)/ Rсм = (4*105 * 0,26)/272,04 = 381,93 K = 108,8 oC
Точка c:
Pc = 4*105 Па
tc = 100 oC = 373,15 K
υc = (Rсм * tc)/ Pc = (273,04*373,15)/4*105 = 0,25 м3/кг
Точка d:
Рd = 7*105 Па
υd = υс/(Pd/Рc)1/k =0,25/(7*105/4*105) = 0,164 м3/кг
td = (Pd* υd)/ Rсм = (7*105 *0,164)/272,04 = 422,35 K = 149,2 oC
Результаты расчета заносим в табл. 1.1.
Таблица 1.1. Параметры газового цикла
|
Точка/Параметры |
P, бар |
υ, |
T, K |
t, |
|
|
a |
6 |
0,1912 |
422,35 |
149,35 |
272,04 |
|
b |
4 |
0,26 |
381,93 |
108,8 |
272,04 |
|
c |
4 |
0,25 |
373,15 |
100 |
272,04 |
|
d |
7 |
0,164 |
422,35 |
149,35 |
272,04 |
2).
Определим
значения средних теплоемкостей ![]() и
и![]() для каждого
процесса.
для каждого
процесса.
Процесс a-b: адиабатный; ![]() =
const, S=const, dq=0
=
const, S=const, dq=0
![]()
![]()
![]()
![]() n
n![]()
![]() =
= ![]()
![]() , значения
, значения ![]() при данной
температуре находим по
при данной
температуре находим по
![]() i=1
i=1 ![]() линейной
интерполяции по таблице средних массовых теплоемкостей различных газов.
линейной
интерполяции по таблице средних массовых теплоемкостей различных газов.
![]() =
=![]() =
= ![]() =
= ![]() =
=
=1,0454
![]()
![]() =
= ![]() =
=![]() =
= ![]() =
=
=0,91686
![]()
![]() =
= ![]() =
=![]() =
= ![]() =
=
=1,906
![]()
![]() =
= ![]() =
= ![]() =
= ![]() =
=
=0,936
![]()
![]() = 0,698;
= 0,698; ![]() = 0,042;
= 0,042; ![]() = 0,03;
= 0,03; ![]() = 0,231
= 0,231
![]() =
=![]() +
+ ![]() +
+ ![]() +
+ ![]() = 1,0454
= 1,0454![]() + 1,906
+ 1,906![]() 0,93
0,93![]() 1,0416
1,0416 ![]()
![]() =
=![]() –
– ![]() = 1041,6 – 272,04
= 768,35
= 1041,6 – 272,04
= 768,35 ![]() =0,77
=0,77 ![]()
Процесс b-c: изобарный; P =const
![]() =
=![]() =
=![]() =
=![]() = 1,0088
= 1,0088 ![]()
![]() =
=![]() =
=![]() =
=![]() =
=
=
1,0542 ![]()
![]() =
= ![]() =
= ![]() =
=![]() =
=
=
1,895
![]()
![]() =
= ![]() =
= ![]() =
=![]() = 0,914
= 0,914 ![]()
![]() =
=![]() +
+ ![]() +
+ ![]() +
+ ![]() = 1,0088
= 1,0088 ![]() + 1,895
+ 1,895![]() 0,914
0,914![]() = 1,0164
= 1,0164 ![]()
![]() =
=![]() –
– ![]() = 1016,4 – 272,04
= 744,363
= 1016,4 – 272,04
= 744,363 ![]() = 0,74
= 0,74 ![]()
Процесс c-d: адиабатный; ![]() =
const, S=const, dq=0
=
const, S=const, dq=0
![]() =
=![]() =
= ![]() =
= ![]() =
=
=1,0388 ![]()
![]() =
= ![]() =
=![]() =
= ![]() =
=
=0,9413 ![]()
![]() =
= ![]() =
=![]() =
= ![]() =
=
=1,904 ![]()
![]() =
= ![]() =
= ![]() =
= ![]() =
=
=0,9321 ![]()
![]() =
=![]() +
+ ![]() +
+ ![]() +
+ ![]() = 1,0388
= 1,0388![]() + 1,904
+ 1,904![]() 0,9321
0,9321![]() 1,037
1,037 ![]()
![]() =
=![]() –
– ![]() = 1037,05
– 272,04 = 765,01
= 1037,05
– 272,04 = 765,01 ![]() =0,765
=0,765
![]()
Процесс d-a: изотермический; T=const
При
t = 149,35 ![]() :
:
![]() = 1,0419
= 1,0419 ![]()
![]() = 0,9292
= 0,9292 ![]()
![]() = 1,8831
= 1,8831 ![]()
![]() = 0,8877
= 0,8877 ![]()
![]() =
=![]() +
+ ![]() +
+ ![]() +
+ ![]() = 1,0
= 1,0![]() + 1,8831
+ 1,8831![]() 0,8877
0,8877![]()
![]()
![]() =
=![]() –
– ![]() = 1027,8 – 272,04
= 755,78
= 1027,8 – 272,04
= 755,78![]() = 0,755
= 0,755 ![]()
3). Найдем изменения внутренней энергии (ΔU), энтальпии (Δi), энтропии (ΔS) в каждом процессе.
Процесс a-b: адиабатный; ![]() =
const, S=const, dq=0
=
const, S=const, dq=0
Δ![]() =
= ![]() (
( ![]() –
– ![]() ) =
0,76955 (381,93 – 422,35) = - 31,1
) =
0,76955 (381,93 – 422,35) = - 31,1 ![]()
Δ![]() =
= ![]() (
( ![]() –
– ![]() ) =
1,0416 (381,93
– 422,35)
= - 42,1
) =
1,0416 (381,93
– 422,35)
= - 42,1![]()
Δ![]() = 0
= 0![]()
Процесс
b-c: изобарный; ![]() =const
=const
Δ![]() =
= ![]() (
( ![]() –
– ![]() ) = 0,7447 (373,15 – 381,93)
= -5,05
) = 0,7447 (373,15 – 381,93)
= -5,05 ![]()
Δ![]() =
= ![]() (
( ![]() –
– ![]() ) = 1,0164 (373,15 – 381,93) = -6,89
) = 1,0164 (373,15 – 381,93) = -6,89 ![]()
Δ![]() =
= ![]() ln
ln ![]() = 1,0164
ln
= 1,0164
ln
![]() = -0,015
= -0,015
![]()
Процесс c-d: адиабатный; ![]() =
const, S=const, dq=0
=
const, S=const, dq=0
Δ![]() =
= ![]() (
( ![]() –
– ![]() ) = 0,76501
(422,35
– 373,15) = 35,84
) = 0,76501
(422,35
– 373,15) = 35,84 ![]()
Δ![]() =
= ![]() (
( ![]() –
– ![]() ) = 1,037 (422,35
– 373,15) = 51,02
) = 1,037 (422,35
– 373,15) = 51,02 ![]()
Δ![]() =
= ![]()
Процесс d-a: изотермический; T=const
Δ![]() =
= ![]()
Δ![]() =
= ![]()
![]()
Δ![]() =
= ![]() ln
ln ![]() = 0,27204
ln
= 0,27204
ln
![]() = 0,042
= 0,042
![]()
Найдем суммарное значение изменения
внутренней энергии (![]() ), энтальпии (
), энтальпии (![]() ) и энтропии (
) и энтропии (![]() ).
).
n
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.