 |
|||
 |
|||
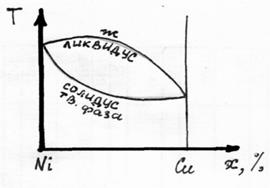
Диаграмма состояния системы из двух компонент в случае полной растворимости.
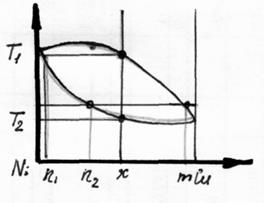
Соотношение жидкой и твердой фаз в процессе кристаллизации определяется пересечением прямой T=const с линиями солидуса и ликвидуса. При медленном (адиабатическом) охлаждении состав закристаллизованного вещества соответствует х. При быстром охлаждении в результате кристаллизации можно получить вещество с неоднородным составом кристаллитов, варьирующимся в пределах, определенных кривыми ликвидуса и солидуса. В последнем случае состав можно частично выровнять за счет отжига (нагрева до температур обеспечивающих большую скорость диффузии).
Как правило, свойства полученных сплавов существенно отличаются от свойств отдельных компонентов. Твердые растворы металлов – это ценный материал для изготовления резисторов, нагревательных и магнитных элементов. Структурой твердого раствора могут обладать и неметаллические вещества, однако неметаллические материалы предпочтительно получать в виде монокристаллов.
 Если условия химического и кристаллографического подобия не выполняются
при затвердевании сплава образовывают смесь кристаллитов различного состава. В
зависимости от способа образовываются такие сплавы делятся на эвтектические и
перитектические.
Если условия химического и кристаллографического подобия не выполняются
при затвердевании сплава образовывают смесь кристаллитов различного состава. В
зависимости от способа образовываются такие сплавы делятся на эвтектические и
перитектические.
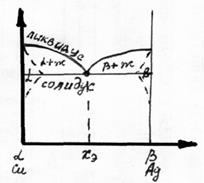
В таком сплаве при понижении температуры начинает кристаллизоваться фаза α (или фаза β) наиболее близкого к х состава, а при температуре равной температуре эвтектики остаток жидкости кристаллизуется в эвтектику (мелкозернистую смесь двух фаз).
Эвтектика окружает кристаллы основной фазы, имеющие правильную геометрическую форму. В точке xэ расплав сразу кристаллизуется в эвтектику. Сплавы эвтектического типа широко применяются для изготовления припоев и металлических клеев. Так, при посадке кремниевых кристаллов на корпус используется сплав Si-Au, образующий жидкую эвтектику при температуре 673 К, которая при охлаждении приваривает кристалл к корпусу. Температура эвтектического сплава много меньше температуры плавления отдельных компонентов сплава, поэтому возникают ограничения на совместное использование различных пар металлов при повышении температуры.
В перитектических сплавах выпавшие первичные кристаллы при дальнейшем понижении температуры может реагировать с оставшимся расплавом с образованием кристаллов другого состава.
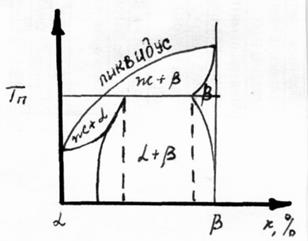 |
При температуре плавления перетектики происходит реакция β+ж=α . Фаза β реагирует с жидкой с выделением α. Полностью закристаллизованное вещество – кристаллы фазы β в окружении кристаллов с фазой α.
Помимо чистых металлов и их сплавов химические элементы – металлы могут образовывать интерметалические соединения. Как правило, компоненты таких соединений расположены достаточо далеко друг от друга в таблице Менделеева. Данные элементы образуют между собой не твердый раствор или расплав а химические соединения с определенной структурной формулой (или ряд химических соединений с близкими структурными формулами), например CuZn, CuZn2, …
Интерметаллические соединения могут иметь связь ионного типа, ионно-ковалентную, ковалентно-металлическую, металлическую. К интерметалличесим относят и ряд химических соединений, один и компонентов которых не является металлом, но которые проявляют свойства металлов, например карбиды (металл-углерод), арсениды (металл-мышьяк ), антимониды (металл-сурьма). Силициды (металл- кремний ) – могут использоваться в качестве основы резистивных сплавов. Среди интерметаллических соединений существуют вещества, способные образовывать сплавы с одним из своих компонентов.
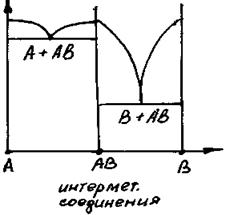
Природным источники металлов могут существовать в самородном виде (Pt, Au, Ag, Cu, St, Hg) либо в виде химических соединений. Из химических соединений металлы извлекают методом восстановительной реакции при большой температуре (пирометаллургия).
Cu2O + C = 2Cu + CO (высокая Т)
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.