Формула (2) применима и к самодиффузии. Определить скорость самодиффузии экспериментально прямым путем до недавнего времени не удавалось. Однако с открытием искусственной радиоактивности положение существенно изменилось, так как оказалось возможным измерить скорость перемещения меченых атомов — радиоактивных изотопов того же самого элемента, вводимых в качестве примеси. Первое применение искусственно радиоактивных изотопов для указанных целей было осуществлено в Ленинграде А. Загрубским (1937), измерившим скорость самодиффузии в золоте. Искусственная радиоактивность создавалась путем облучения обычного золота нейтронами от радий-бериллиевого источника. Слой радиоактивного золота электролитически наносился на поверхность золотой пластинки. Скорость самодиффузии после прогрева при разных температурах определялась по уменьшению активности препарата.
Коэффициент самодиффузии золота
T,К 1073 1173 1273
D, см2/сутки 2,3*10-7 5,0.10-7 1,4.10-5
Опытные данные для коэффициента самодиффузии золота приводят к формуле
D =7,94*105e 62900/RTсм2/сутки. (XV.4)
Работа активации самодиффузии Q = 62,9 ккал/моль составляет около 2/3 полной энергии сублимации золота (L = 92,0 ккал/моль при комнатной температуре).
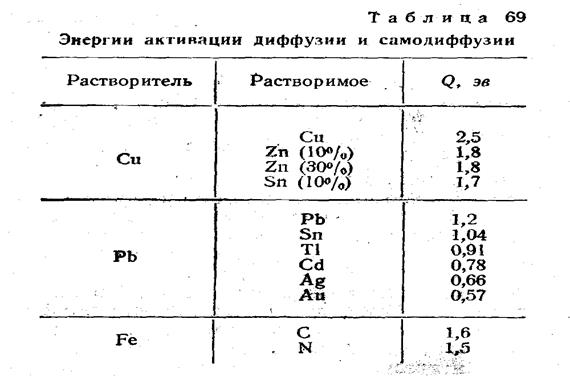
Энергии активации диффузии и самодиффузии для некоторых металлов приведены в табл. 69. Эти энергии для различных атомов при диффузии в одном и том же растворителе значительно отличаются. Чем больше химически различаются растворитель к диффундирующие атомы, тем энергии диффузии меньше. Наибольшие значения в соответствующих рядах имеют энергии самодиффузии. Эту закономерность можно объяснить тем, что при уменьшении химического различия атомов прочность связи атомов в решетке должна увеличиваться.
Углерод и азот в железе образуют твердый раствор внедрения. Диффузия этих атомов в решетке железа, проходящая с заметной скоростью, показывает возможность диффузионного перемещения атомов по междуузлиям. Скорость диффузии зависит от состояния материала (величины зерна, внутренних напряжений). Скорость диффузии тория в вольфраме заметно возрастает с уменьшением величины зерен вольфрама. Это показывает, что атомы
тория преимущественно диффундируют по границам кристаллов. Для диффузии цинка в меди зависимость скорости от величины зерна не наблюдается. Атомы цинка диффундируют как по границам, так и через кристаллы меди. Скорость диффузии цинка в меди существенно зависит от состава сплава. По мере увеличения концентрации цинка будут образовываться соединения промежуточного состава (фазы β, γ, ε). Вдоль диффузионного потока установится распределение фаз (рис. 252), соответствует диаграмме состояния медь — цинк.Скорость диффузии цинка в различных фазах различна.
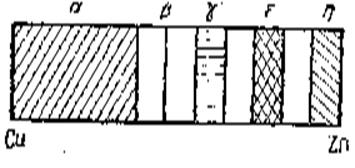
Рис. 254. Распределение фаз в диффузионном потоке.
МЕХАНИЗМ ДИФФУЗИИ В КРИСТАЛЛАХ
Возможны различные перемещения атомов в кристаллической решетке. Для кристалла с идеальной ненарушенной структурой, при условии сохранения этой идеальной структуры, возможны два способа диффузии (рис. 253): а) одновременный обмен местами пары атомов 2 и 2 и б) кольцевая диффузия, когда одновременный обмен местами совершает большая группа атомов.
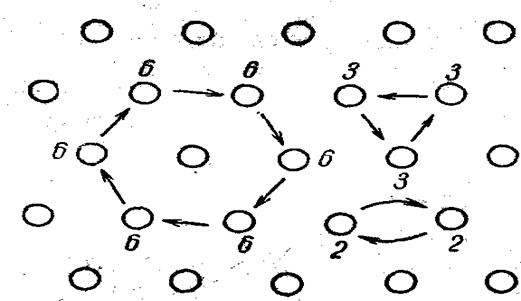
Рис. 253. Диффузия по механизму обмена атомов местами (обмен двух атомов, трех атомов и шести атомов)
На рис. 253 показаны примеры кольцевой диффузии для треугольника и шестиугольника. Для плотно упакованного шарового слоя группа из шести атомов образует правильный шестиугольник, приближающийся к кольцу. Одновременный обмен местами пары атомов в плотно упакованной структуре требует преодоления большого потенциального барьера, связанного с раздвижением соседних атомов. При групповом перемещении атомов в кольцевом механизме диффузии доля энергии потенциального барьера, приходящаяся на один атом, будет соответственно меньше, чем при обмене пары атомов местами. Однако эта энергия возрастает с увеличением числа атомов в кольце и вероятность осуществления такого процесса за счет флуктуационного накопления необходимой тепловой энергии резко падает.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.