Федеральное агентство по образованию РФ
Государственное образовательное учреждение высшего профессионального образования
"Владимирский государственный университет"
Кафедра конструирования и технологии радиоэлектронных средств
Лабораторная работа № 1
Исследование диаграмм кипения двухкомпонентной системы
Выполнил: студент группы Р-107
Принял:
Владимир 2010
Цель работы: исследовать диаграммы кипения двухкомпонентной системы.
Исходные данные.
В таблице 1 дана зависимость составов жидкой (Х) и газообразной (У) фаз от температуры (Т) для бинарной жидкой системы А-В при постоянном давлении Р.
Таблица 1
Исходные данные
|
А – C2H6O B – C6H6 |
состав А, мол. % |
Т, К |
Р, кПа |
|
|
Раствор, Х |
Пар, У |
|||
|
0 |
0 |
352,8 |
100 |
|
|
4,0 |
15,1 |
348,2 |
||
|
15,9 |
35,3 |
342,5 |
||
|
29,8 |
40,5 |
341,2 |
||
|
42,1 |
43,6 |
340,8 |
||
|
53,7 |
46,6 |
341,0 |
||
|
62,9 |
50,5 |
341,4 |
||
|
71,8 |
54,9 |
342,0 |
||
|
79,8 |
60,6 |
343,3 |
||
|
87,2 |
68,3 |
344,8 |
||
|
93,9 |
78,7 |
347,4 |
||
|
100 |
100 |
351,1 |
||
Лабораторное задание.
1. Построение диаграммы состав пара-состав раствора.
Построенная по исходным данным и аппроксимированная зависимость состава пара от состава раствора представлена на рис. 1.
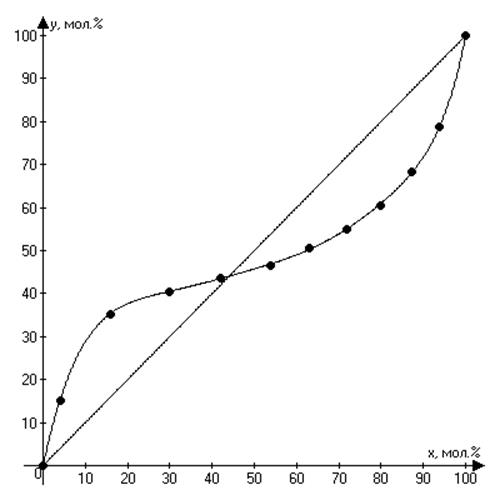
Рис. 1. Зависимость состава пара от состава жидкой фазы
График пересекает функцию y=x в точке x=44%, следовательно, азеотропная смесь на 44% будет состоять из этанола и на 56% из бензола.
2. Построение диаграммы состав-температура кипения.
Зависимость состав-температура кипения представлена на рис. 2. Сплошной линией показан график жидкой фазы, штриховой линией – пара.
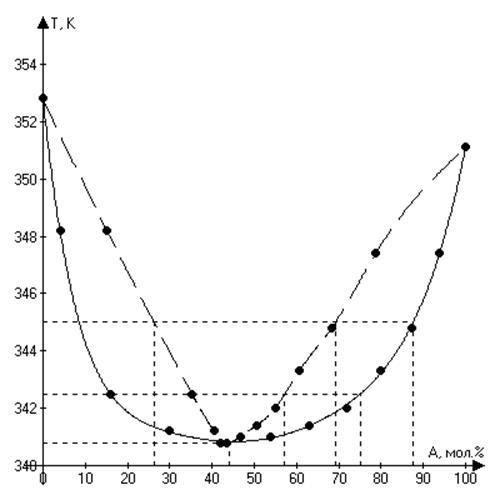
Рис. 2. Зависимость состав-температура кипения
3. Определить температуру кипения системы, содержащей 75 мол.% компонента А; каков состав первого пузырька пара, при какой температуре исчезнет последняя капля жидкости и каков ее состав.
Температуру кипения системы, содержащей 0,75 мол. долей компонента А (этанола), можно определить по рис. 2. Для этого надо найти проекцию точки 0,75 на графике для раствора на ось температур. Таким образом, температура кипения заданной смеси будет равна 342,5 К.
Первый пузырек пара будет иметь следующий состав: C6H5O – 57,2 мол.%, C6H6 – 42,8 мол. %. Это определяется по найденной температуре кипения и графику для пара.
Согласно законам Коновалова, последняя капля жидкости исчезнет в азеотропной системе, т.е. её температура и состав будут определяться точкой касания диаграмм для жидкости и пара. Согласно рис. 2 последняя капля исчезнет при температуре 340,8 К, её состав – 44% метанола, 56% бензола.
4. Определить состав пара, находящегося в равновесии с жидкой бинарной системой, кипящей при 345 К.
Состав пара, находящегося в равновесии с жидкой бинарной системой, кипящей при Т = 345 К, определяется по рис. 2. Возможны два случая в зависимости от состава исходного раствора.
Если состав раствора: C2H6O ≈ 9 мол. %, C6H6 ≈ 91 мол. %, тогда состав равновесного пара C2H6O = 26,6 мол. %, C6H6 = 73,4 мол. %.
Если состав раствора: C2H6O ≈ 87,6 мол. %, C6H6 ≈ 91 мол. %, тогда состав равновесного пара C2H6O = 69,2 мол. %, C6H6 = 30,8 мол. %.
5. При помощи какого эксперимента можно установить состав жидкой бинарной системы, если она начинает кипеть при 345 К (при наличии диаграммы состав-температура кипения).
Для того чтобы установить состав жидкой фазы бинарной системы необходимо провести ректификацию (испарение – конденсация - испарение и т.д.) до получения чистого компонента А или В. В зависимости от того какой компонент выделится по диаграмме кипения определяется с какой стороны от азеотропной точки имеет место состав раствора при Т1=345 К.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.