3. Технологическая часть.
3.1. Теоретические основы процесса.
3.1.1. Равновесие реакции синтеза
Синтез аммиака из азота и водорода
1/2N2 + 3/2Н2 Û NH3 + Q
относится к числу равновесных обратимых реакций, протекающих с выделением тепла и уменьшением объема. Согласно принципу Ле-Шателье, равновесной степени превращения исходных веществ увеличивается с повышением давления и понижением температуры [1-4].
3.1.2. Тепловой эффект реакции
Тепловой эффект реакции синтеза аммиака в реальных условиях проведения процесса состоит из двух слагаемых [1]:
Q = Qp + Qсм (3.11)
где Qр—тепловой эффект реакции при полном превращении азотоводородной смеси в аммиак; Сcм — теплоты смешения аммиака с азотоводородной смесью. Qp и Qсм, а следовательно и Q, зависят от температуры и давления. Значения Qp можно рассчитать по уравнению [1]
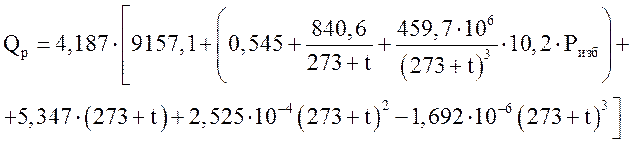 (3.12)
(3.12)
где
Р — избыточное давление, МПа; ![]() — температура, °С.
— температура, °С.
Теплоты смешения (Qсм) при разных давлениях, температурах и концентрации аммиака в смеси (17,6; 20; 40; 80% МН3) были определены Я. С. Казарновским и др. Qсм, в отличие от QР, является отрицательной величиной, так как при смешении сжатых азота, водорода и аммиака происходит поглощение тепла.
3.1.3. Кинетика синтеза аммиака
Синтез аммиака из азота и водорода протекает с заметной скоростью только в присутствии катализатора. Скорость синтеза аммиака на большинстве известных катализаторов описывается уравнением Темкина — Пыжева [1-3]
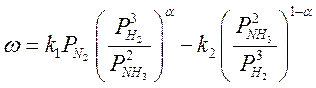 (3.17)
(3.17)
где w — наблюдаемая скорость реакции, равная разности скоростей образования и разложения аммиака; k1 k2 — константы скорости образования и разложения аммиака (отношение k1/k2=KР, где KР — константа равновесия); Рн2, PN2, рNнз — парциальные давления водорода, азота и аммиака; a — постоянная, удовлетворяющая неравенству 0<a<1.
Bпромышленных условиях, особенно на крупных зернах катализатора, значительное влияние на скорость процесса оказывает диффузионное торможение, которое возрастает с повышением температуры и уменьшением содержания аммиака в газе на входе, увеличением активности катализатора.
3.2. Описание технологической схемы
Компримирование синтез-газа.
Очищенный от СО и СО2 синтез-газ с температурой не более 43 °С и давлением до 2,53 МПа поступает на всас трехкорпусного компрессора синтез-газа, имеющего четыре ступени для сжатия синтез-газа и ступень для сжатия циркуляционного газа.
В первой ступени корпуса низкого давления газ сжимается до давления 5,17 МПа, нагреваясь при этом до температуры не более 140 °С, и направляется в теплообменник, где охлаждается до температуры не более 85 °С, нагревая газ, идущий на метанатор.
Затем газ поступает в воздушный холодильник, где охлаждается до температуры не более 49 °С, проходит сепаратор и поступает на всас второй ступени компрессора.
Во второй ступени компрессора синтез-газ сжимается до давления не более 9,81 МПа и с температурой не более 150 °С поступает в воздушный холодильник, где охлаждается до температуры не более 49 °С. Для связывания диоксида углерода и влаги в линию газа перед холодильником насосами из сборника впрыскивается жидкий аммиак.
После воздушного холодильника синтез-газ поступает в аммиачный холодильник, где за счет испарения аммиака в межтрубном пространстве температура газа снижается до 5¸8 °С.
Отделение сконденсировавшейся жидкости из охлажденного газа производится в сепараторе, откуда конденсат выводится в отпарную колонну, а газ поступает на всас третьей ступени компрессора с давлением не более 9,81 МПа и температурой не более 8 °С.
В третьей ступени (корпус среднего давления) газ сжимается до давления не более 21,58 МПа, нагреваясь при этом до температуры не более 119 °С. После третьей ступени газ поступает в воздушный холодильник, где охлаждается до температуры 49 °С и направляется для отделения сконденсировавшейся влаги в сепаратор, откуда конденсат выводится в отпарную колонну, а газ идет на всас четвертой ступени компрессора.
Из сепаратора газ идет на всас четвертой ступени компрессора (корпус высокого давления).
После четвертой ступени газ выходит с давлением не более 32,96 МПа и температурой не более 128 °С и направляется в воздушный холодильник.
В корпусе высокого давления компрессора расположена циркуляционная ступень, служащая для дожатия синтез-газа после колонны синтеза до рабочего давления.
На всас циркуляционной ступени газ поступает с температурой не более 21 °С. Сжимается здесь до давления не более 32,96 МПа, нагреваясь до температуры 30-32 °С.
На случай разгрузки системы синтеза в схеме компрессора предусмотрен байпас с общего нагнетательного коллектора свежего и циркуляционного газа на всас циркуляционной ступени компрессора.
При работе компрессора в корпусе высокого давления возможно создание условий, благоприятных для образования карбоната или карбомата аммония из СО2, NH3 и Н2О, содержащихся в свежем газе. Поэтому снижение температуры на всасе четвертой ступени не допускается ниже 43 °С, так как отложение солей на роторе и корпусе компрессора могут привести к недопустимой вибрации и разрушению компрессора. Минимальная температура на всасе по ступеням компрессора сигнализируется в ЦПУ.
Синтез аммиака и аммиачное охлаждение.
Смесь свежего и циркуляционного
газов после компрессора с температурой не более 40 °С, давлением не более 32,96
МПа и объемной долей аммиака до 5 % направляется в аммиачный холодильник 14
для охлаждения до температуры 0![]() 4 °С.
4 °С.
Сконденсировавшийся в газе аммиак отделяется в сепараторе 1. Жидкий аммиак, отделившийся в сепараторе 1 выводится в сборник 2. Для улучшения сепарации аммиака внутри сепаратора 1 смонтирован циклон, состоящий из пакета труб. Накапливающийся в циклоне жидкий аммиак через дренажный вентиль перепускается в первичный сепаратор 3.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.