Содержание:
1.Гистидин.
2.Биосинтез гистидина.
3.Биологическая роль гистидина.
4.Пути обмена гистидина.
5.Карнозин и ансерин.
6.Патология и фармакологическое применение.
7.Список используемой литературы.
1.Гистидин
Гистидин. Пути расщепления гистидина были выяснены только в последнее время, хотя уроканиновую кислоту изолировали из мочи собак уже сравнительно давно. Гистидин сначала под действием гистидинаммшк-лиазы дезаминируется (в боковой его цепи), а потом окисляется (его имида-зольное кольцо) и после всего этого происходит разрыв его кольца с образованием формиминоглютаминоеой кислоты (формамидиноглютаровой кислоты). Это последнее соединение (по первому названию) содержит один радикал —CH=NH (формиминогруппа), присоединенный к аминогруппе глютами-новой кислоты. Формиминогруппа способна связаться с ТГПГ в виде фор-мимино-ТГПГ, который превращается в метенил-ТГПГ с освобождением аммиака. Таким образом, 2-й С-атом имндазольного кольца гистидина составляет часть запаса активного Ct организма. Описанный путь расщепления гистидина схематично выглядит следующим образом:
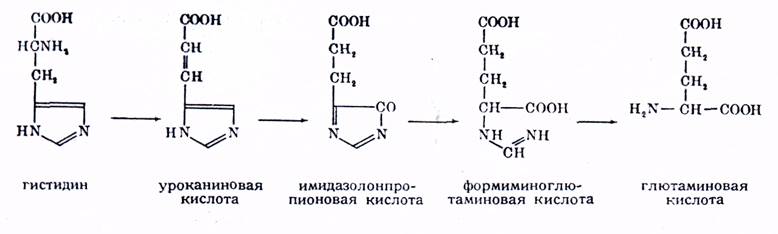
2.Биосинтез гистидина
Биосинтез гистидина. Для человека гистидин является неэссенци-альной (заменимой) аминокислотой. Не слишком продолжительное отсутствие его в пище не вызывает никаких расстройств в организме. Механизм биосинтеза гистидина в высокоорганизованных организмах еще не выяснен, но можно предположить, что ход реакции по существу не отличается от синтеза его в микроорганизмах [Мойед, Магасаник (Moved, Magasanik)]. При исследованиях исходили из того наблюдения, что первый (N) и второй (С) атомы гистидин получает из аденина (1. N и 2. С последнего), но 3. N-ато.м гистидина доставляется глютамином (его амидным азотом). С другой стороны, уже давно установлено, что гистидин образуется из гистидинола.
Очень интересно то, что аденин, содержащий имидазольное кольцо, принимает участие в синтезе гистидина не своим имидазольным кольцом. Образующееся при разрыве аденина соединение — аминоимидазолкарбокса-мидриботид — является промежуточным продуктом биосинтеза пуриновых оснований, который при использовании активного С1 может переходить в инозиновую кислоту и через последнюю в адениловую кислоту.
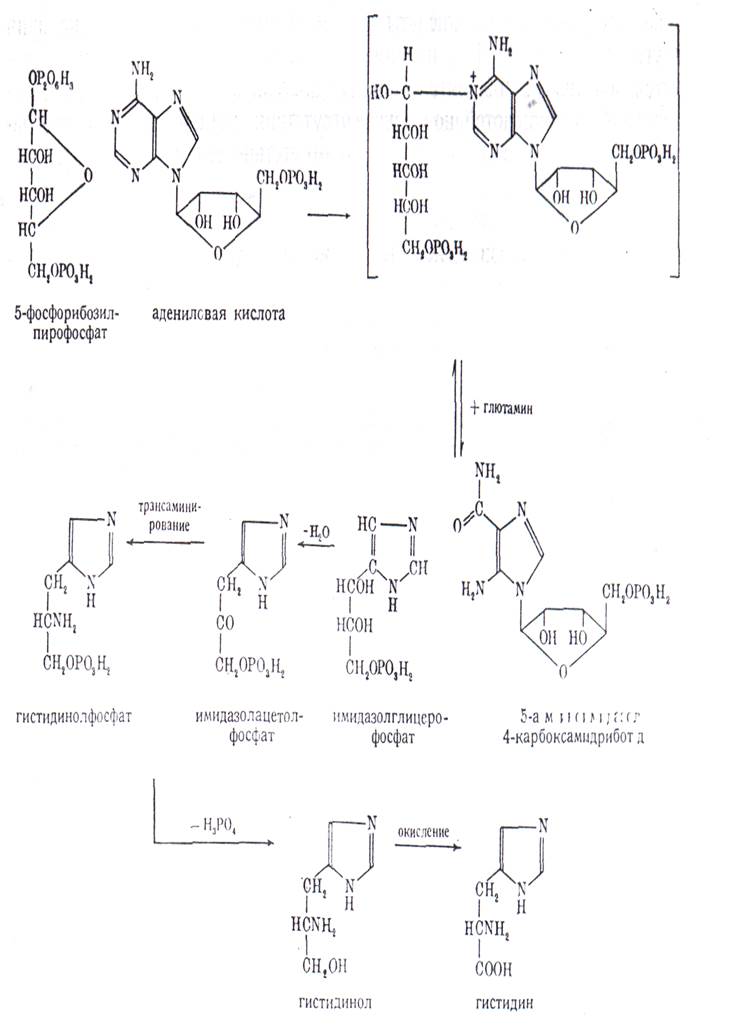
БИОСИНТЕЗ ГИСТИДИНА
3.Биологическая роль гистидина
Способность взрослого человека обходиться без гистидина в пище может быть связана с тем, что гистидин синтезируется у него в кишечнике микроорганизмами и оттуда всасывается в кровь. Возможно, что организм взрослого человека обходится очень малыми количествами гистидина и образование его микрофлорой кишечника достаточно для удовлетворения его потребности.
Имидазольное ядро гистидина в организме животных расщепляется. Установлено, что в печени содержатся ферменты, объединенные под названием гистидаза, способные расщеплять имидазольное ядро гистидина с образованием молекулы глутаминовой кислоты, молекулы муравьиного альдегида и двух молекул аммиака.
В выяснении пути расщепления в организме гистидина выдающуюся роль сыграли опыты с применением изотопов. Гистидин в этих опытах метился в различных частях своей молекулы С14 и N15.' Меченые молекулы гистидина вводились в организм, а затем изучалось появление изотопов в предполагаемых промежуточных продуктах распада гистидина. Результаты этих опытов показали, что начальной реакцией превращения гистидина является его дезаминирование при участии фермента гистидиндеза-миназы с образованием уроканиповон кислоты и аммиака.
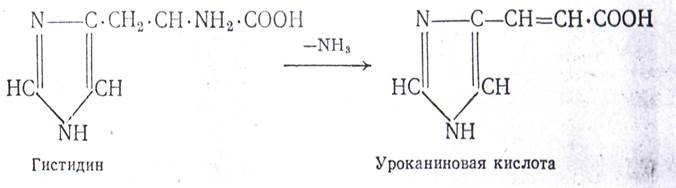
Уроканиновая кислота под влиянием уроканиназы подвергается дальнейшему расщеплению с выделением формамидглутаминовой кислоты.
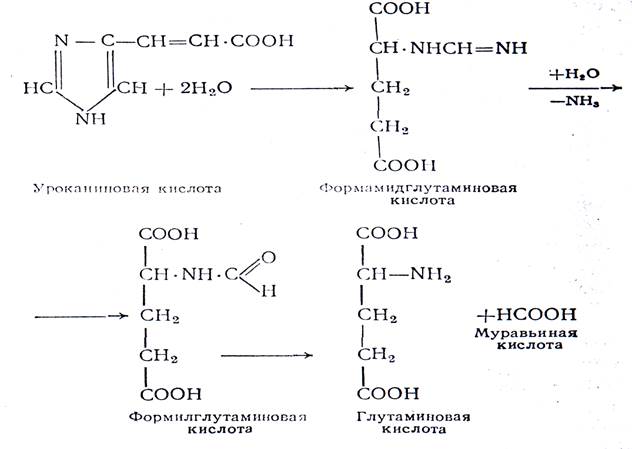
Формилглутаминовая кислота расщепляется с образованием глутаминовой и муравьиной кислот.
Образование глутаминовой кислоты сближает обмен гистидина с обменом углеводов в организме, а образование муравьиной кислоты—с обменом глицина и серина. У двустворчатых моллюсков превращение гистидина происходит без промежуточного образования уроканиновой кислоты. У них гистидин теряет а-аминогруппу с образованием имидазолпировиноградной кислоты, которая, декарбоксилируясь, превращается в имидазолуксусную кислоту и в иные имидазолсодержащие соединения.
В организмах встречаются производные гистидина, имеющие в своем составе имидазольное ядро. Среди них особенно интересен гистамин, образующийся при декарбоксилироваиии гистидина микроорганизмами, а также ферментами ряда тканей животных. Гистамин в очень малых количествах обнаружен в связанном состоянии в различных тканях (легких, печени, слизистой оболочке желудка и др.). Гистамин освобождается из связанной формы в плазмоцитах (тучных клетках) при анафилактическом шоке и с действием его, в известной мере, связано проявление шока. Гистамин понижает кровяное давление, стимулирует функции желез внешней секреции (усиливает секрецию желудочного и иных соков). Гистамин в организме подвергается окислительному дезаминированию
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.