Легкость нуклеофильной атаки зависит от величины эффективного положительного заряда атома углерода карбонильной группы. В функциональных производных карбоно
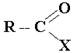 |
вых кислот он увеличивается с ростом –I-эффекта заместителя и уменьшается с усилением его +М-эффекта.
Получение функциональных производных карбоновых кислот (SN)
1. Получение сложных эфиров (реакция этерификации).
Реакция этерификации в отсутствии катализаторов протекает чрезвычайно медленно. Однако в присутствии минеральных кислот (Н2SO4,, HCl) реакция существенно ускоряется.
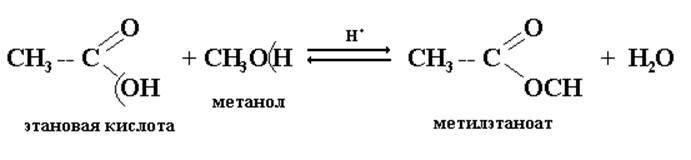
Функцией катализатора является повышение электрофильность атома углерода карбоксильной группы путем протонирования карбонильного атома кислорода и образование карбокатиона:
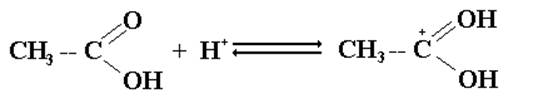
карбокатион
Процесс этерификации обратим.
2. Получение аминов карбоновых кислот.
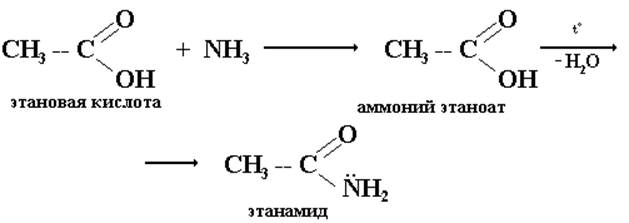
За счет взаимодействия неопределенной пары электронов атома азота с π-электронами поляризованной двойной связи карбонильной группы, связь C – N в амидах имеет часто двойной характер.
Амиды карбоновых кислот в зависимости от степени замещения у атома азота, могут быть первичными RCONH2, вторичными RCONHR' и третичными. По сравнению с другими производными карбоновых кислот, амиды наиболее склонны к реакциям нуклеофильного замещения.
3. Получение галогенангидридов
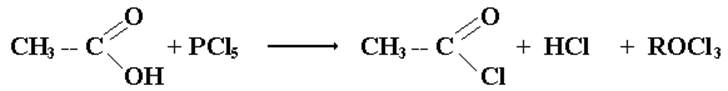
этановая кислота хлорангидрид этановой кислоты
Галогенангидриды наиболее активны в SN-реакциях.
4. Получение ангидридов – 2 способа:
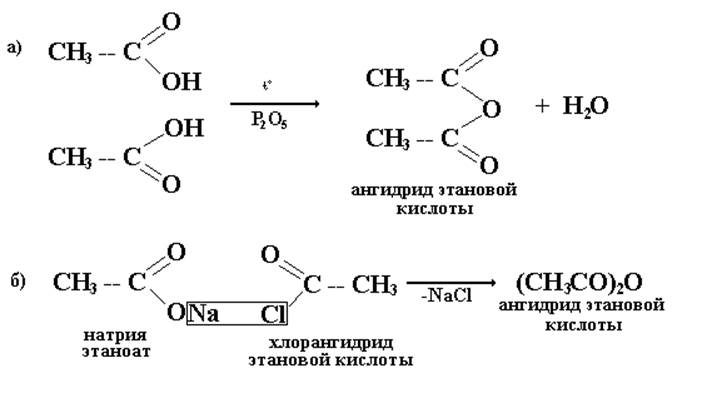
Путем взаимных превращений можно переходить от одних функциональных производных к другим. Большая часть этих превращений представляет собой реакции ацилирования, то есть введения ацильной группы RCOˉ в молекулу вместо атома водорода.
Процессы гидролиза функциональных производных карбоновых кислот, а также их взаимопревращений протекает по механизму SN.
Способность к гидролизу и реакционная способность в SN-реакциях зависит от эффективного положительного заряда на карбонильном атоме углерода в соединениях RCO – X, величина которого определяется природой Х, то есть совместным действием его –I- и +М-эффектов. Поэтому по легкости гидролиза функциональные производные карбоновых кислот в соответствии со своей ацилирующей способностью располагаются в следующий ряд:
Взаимопревращения функциональных производных
карбоновых кислот (SN)
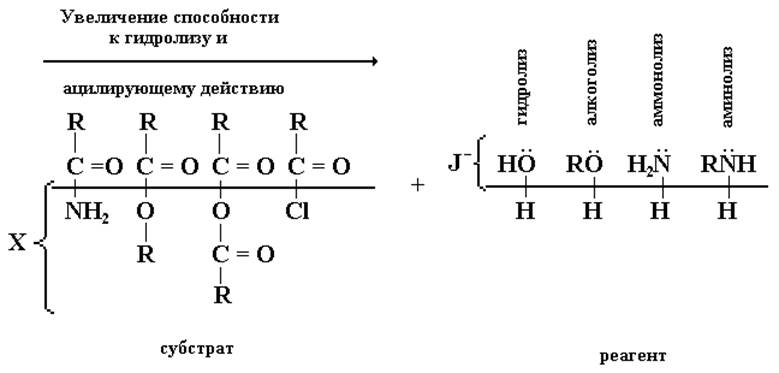
Так, например, сложные эфиры могут подвергаться гидролизу, как в кислой, так и в щелочной средах. Гидролиз в щелочной среде необратим и требует эквивалентного количества щелочи.
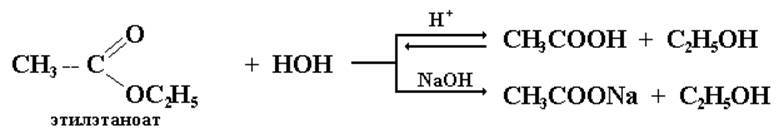
Так как амиды, по сравнению с другими производными карбоновых кислот, наименее склонны к реакциям нуклеофильного замещения, то их гидролиз осуществляется в достаточно жестких условиях (многочасовое кипячение с концентрированными водными растворами кислот или щелочей).
Особенности поведения двухосновных карбоновых кислот
Двухосновные карбоновые кислоты обладают более кислым характером, чем одноосновные и образуют два ряда функциональных производных – по одной и двум карбоксильным группам, которые можно получить общими для карбоновых кислот методами.
Расположение двух электроноакцепторных групп в непосредственной
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.