Рис. 74. Растворимость водорода в жидких железоуглеродистых сплавах:
1 - по данным [239]; 2 - по данным [242]; 3 - по данным [243]
Рис. 75. Совместная растворимость водорода и кислорода в жидком железе при 5мм рт. ст.
Вопрос о состоянии водорода в железе многократно обсуждался в литературе. Первоначальное представление о возможности образования гидридов при окклюзии водорода железом не подтвердилось экспериментами, и в настоящее время большинство исследователей не разделяет этой точки зрения. Точно так, же оказалось ошибочным и представление о системе водород-железо как о твердом растворе внедрения. Наиболее приемлемой гипотезой, основанной на работах А. И. Красникова, Н. А. Галактионовой, В. И. Явойского и других, является представление о присутствии водорода в твердом и расплавленном железе в форме протона в электронных оболочках металлических атомов. Данные этих работ были изложены в гл. П. Последующие работы также подтвердили правильность изложенных представлений. М. М. Швед и Г. В. Карпенко произвели измерения работы выхода электронов из поликристаллического α -железа до и после электролитического наводороживания при комнатной температуре. Измерения показали, что поглощение водорода приводит к уменьшению работы выхода электронов. С увеличением времени насыщения и, следовательно, количества поглощенного водорода работа выхода резко падает, достигая минимального значения при продолжительности насыщения около 20 мин. Увеличение плотности тока также приводит к уменьшению работы выхода электронов. Вылеживание образцов при комнатной температуре после наводороживания приводит к увеличению работы выхода и после 24 ч старения работа выхода восстанавливается до первоначального значения. Так как возникающие при наводороживании внутренние напряжения уменьшают работу выхода, по полученным данным, в значительно меньшей степени, авторы считают, что протоны водорода в решетке металла создают двойной электрический слой, понижающий работу выхода. При старении навод6роженного образца происходит диффузия протонов через решетку к поверхности и десорбция водорода из металла, что облегчает выход электронов. И. С. Слабковский и Р. И. К:рипякевич изучили влияние водорода, растворенного в решетке железа, на положение и структуру линии Kβ, и подтвердили, что водород сильно влияет на энергетические уровни атома металла: наблюдались значительные смещения линии Kβв длинноволновую сторону, а также изменения ширины и формы линии.
Особо следует остановиться на вопросе о диффузии и десорбции водорода в железе. В настоящее время является полностью доказанным и общепризнанным, что водород диффундирует через кристаллическую решетку железа как протон.
Среднее значение константы диффузии для системы водород-железо указывается равным 2,40·10-3. Борелиус и Линдблом дают несколько меньшую величину, равную 1,60·10-3. Такую же цифру (1,63·10-3) называют Смиттелс и Ренслей. Бастьен и Азу определили коэффициент диффузии водорода и дейтерия в отожженной стали, содержащей 0,08% С; 0,29% Si и 0,35% Мn. Существенного различия в коэффициентах диффузии водорода и дейтерия в стали не было обнаружено: в одинаковых условиях опыта коэффициент диффузии дейтерия составил DО = 1,1 ∙ 10-7 см2/сек, а водорода Dи = 1,25· 1O-7 см2/сек. Однако изучение поглощения водорода и дейтерия сталью в процессе нанесения гальванических покрытий с применением Н2О и D20 В качестве растворителей, произведенное в недавней работе Вуда, показало, что дейтерий поглощается сталью из электролита значительно интенсивнее, чем водород. Полученные Вудом данные приведены на рис. 76.
С повышением давления и температуры скорость диффузии водорода в железе возрастает.
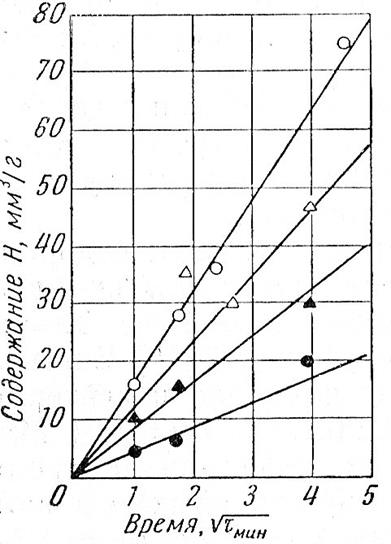
Рис. 76. Поглощение водорода и дейтерия сталью при нанесении электролитических покрытий:
Покрытие Газ Н2 D2
Кадмий ….. …………….....• ◦
Медь …… ...……………...▪ ▫
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.