Министерство образования Российской Федерации
Новосибирский Государственный Технический Университет
Кафедра «Технологические процессы и аппараты»
Отчет по преддипломной практике
5 курса, группы КХ-501
По теме: «Гидротермальный синтез основного олеата висмута (III)».
Преддипломная практика проходила в лаборатории порошковых материалов ИХТТиМ СО РАН
Научный руководитель
Удалова Татьяна Александрова
к.х.н., н.с.; лаборатория порошковых материалов ИХТТиМ
Новосибирск 2010
Оглавление
Цель работы: 3
Экспериментальная часть. 4
Определение свободной кислоты.. 5
Определение нитратов. 5
Результаты исследований. 6
Основной результат преддипломной практики: 7
определение возможности гидротермального синтеза основного олеата висмута из азотнокислых растворов, широко применяемых в технологии соединений висмута.
Основной промышленный способ получения соединений висмута, как с органическими, так и с неорганическими анионами, - гидролитическое осаждение. Для исследования составов осаждаемых соединений висмута целесообразно использовать хлорнокислые растворы, в которых висмут не образует комплексов с перхлорат-ионами. Такие системы были исследованы для изучения химического состава синтезированного нами ранее основного олеата висмута.
В промышленности традиционно используются азотнокислые растворы, в которых происходит образование осадков смешанных гидроксокомплексов висмута, содержащих анионы минеральных кислот. Это вызывает необходимость изучения условий и состава продуктов осаждения из азотнокислых растворов для разработки промышленного способа синтеза основного олеата висмута.
Работа состояла из этапов:
I. Освоение аналитических методик определения:
1) свободной кислоты в технологических висмутсодержащих азотнокислых растворов
2) нитрат-ионов в продуктах гидротермального осаждения
II. Исследование влияния концентрации:
1) олеат-ионов,
2) температуры процесса,
3) концентрации ионов водорода в растворе на степень осаждения висмута из азотнокислых растворов и состав образующихся соединений.
III. Анализ водных фаз на содержание:
1) катионов висмута Bi3+
2) нитрат-ионов NO3-
3) свободной кислоты H+
IV. Анализ продуктов осаждения на содержание:
1) катионов висмута Bi3+
2) нитрат ионов NO3-
3) олеат-ионов (по содержанию углерода).
В работе использовали реактивы квалификации “хч” или “ос.ч”. Исходные растворы готовили растворением оксида висмута квалификации “ос.ч. 13-3” в азотной кислоте с концентрацией 7 моль/л. Гидролитическое осаждение оксид-олеат висмута вели в термостатированых стеклянных или фторопластовых сосудах, снабженных мешалками, на водяных банях, добавлением висмутсодержащего азотнокислого раствора к водному раствору олеата натрия или олеиновой кислоты. Смесь перемешивали в течение 1ч. Осадок отфильтровывали, промывали дистиллированной водой, водно-спиртовым раствором (1:1) и сушили на воздухе.
Анализ продуктов осаждения методами химического и рентгенофазового анализов, ИК–спектроскопии, термогравиметрии, электронно-микроскопические снимки выполнены в ИХТТиМ СО РАН.
MAX, 1970 №12 стр.2447
5-10 мл 5% раствора Трилона Б помещают в коническую колбу на 250 мл, приливают в колбу 2-4 мл 10 % раствора CaCl2, 5-6 капель метилового красного, 80 мл H2Oдист. и нейтрализуют NaOH до изменения окраски от красного до соломенно желтого цвета. К полученному раствору добавить a мл исследуемого раствора и титровать его установленным раствором NaOH до анологичного изменения окраски индикатора.
Реактивы:
10% раствор CaCl2
5% Трилон Б
Индикатор метиловый оранжевый
NaOH – 2M и 0,2 (0,1) N
Расчет свободной H+ по методике Поляка:
[H+] = CNaOH · VNaOH (мл) / a (исследуемого раствора) мл
Метиловый красный C15H15O2N3
Спиртовый раствор: 0,1 г препарата растворяют при нагревании в 100 мл этанола.
1. Приготовление основного стандартного раствора KNO3
0,145 г KNO3 растворить в дистиллированной воде в колбе на 100 мл
2. Приготовление рабочего стандартного раствора KNO3
5 мл основого раствора разбавить в мерной колбе дистиллированной водой до 100 мл
3. 0,5 % раствор NaSal (0,5 в 100 мл)
4. 10 н раствор NaOH (80 г в 200 мл)
По данным химического анализа продуктов осаждения висмута из азотнокислых растворов олеата натрия при 65ºС и варьировании величины n от 0.25 до 4.0 (реакция среды раствора изменяется от pH от 0.93 до pH 2.19 соотвественно), осадки полученные после предварительной промывки этиловым спиртом представляют собой оксид-олеат висмута BiО(С18Н33О2).Содержание нитрат-ионов в осадках составляет 4.0-1.5%.Однократная промывка полученного осадка при 65ºС, согласно данным РФА. Не влияет на его состав, при этом содержание нитрат-ионов в осадке снижается до 1.45%.Промывка полученного осадка раствором олеат натрия (0.1 моль/л) при 65ºС, а затем дистиллированной водой позволяет очистить его от нитрат-ионов и снизить их содержание с 4.0 до 0.07 %.
Проведенные исследования по осаждению основного олеата висмута из азотнокислых растворов при 25 ±1ºС и 65±5ºС растворами олеата натрия или олеиновой кислоты при 25±5ºС и 65±5ºС показали, что степень осаждения висмута (R) с ростом концентрации олеат-ионов и повышением температуры процесса увеличивается. При молярном соотношении олеат – ионов к висмуту в растворе (n), равном 1,0, степень осаждения висмута составляет , %: 97.89(1), 96.21 (2), 95.82 (3), 90.77(4) (см.рис.1).
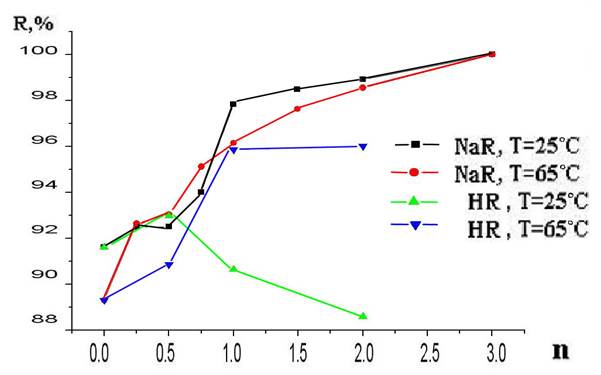
Рис.1. Зависимость степени осаждения R % висмута (III) от молярного соотношения олеат-ионов и висмута (n)
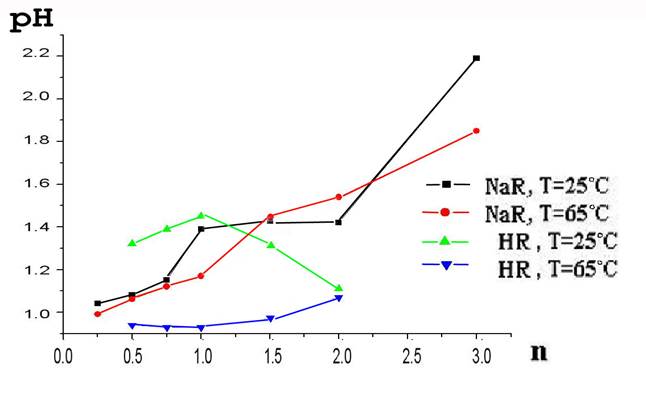
Рис.2. Зависимость степени осаждения pH от молярного соотношения олеат-ионов и висмута (n)
Показана возможность синтеза основного олеата висмута из азотнокислых растворов в промышленных условиях.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.