2) С2Н6 = С2Н2 + 2Н2
30 26 4 Х=1,643
2,528·0,75 Х Y Y=0,253
3) С3Н8 = 1,5С2Н2 + 2,5Н2
44 39 5 Х=3,287
4,945·0,75 Х Y Y=0,421
4) С4Н10 = 2С2Н2 + 3Н2
58 52 6 Х=2,191
3,258·0,75 Х Y Y=0,253
5) С5Н12 = 2,5С2Н2 + 3,5Н2
72 65 7 Х=1,096
1,619·0,75 Х Y Y=0,118
3. Определяем количество углерода (в виде сажи) и водорода, кг
1) СН4 = С + 2Н2
16 12 4 Х=5,043
84,054·0,08 Х Y Y=1,681
2) С2Н6 = 2С + 3Н2
30 24 6 Х=0,162
2,528·0,08 Х Y Y=0,041
3) С3Н8 = 3С + 4Н2
44 36 8 Х=0,324
4,945·0,08 Х Y Y=0,072
4) С4Н10 = 4С + 5Н2
58 48 10 Х=0,216
3,258·0,08 Х Y Y=0,045
5) С5Н12 = 5 С + 6Н2
72 60 12 Х=0,108
1,619·0,08 Х Y Y=0,022
4. Определяем количество этилена и водорода, кг
1) СН4 = 0,5С2Н4 + Н2
16 14 2 Х=4,413
84,054·0,06 Х Y Y=0,630
5. Определяем количество плазмообразующего газа. Объем природного газа 100 кг.
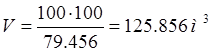
Поскольку удельному расходу природного газа 1,466 м3/с соответствует удельный расход плазмообразующего газа 0,87 м3/с, то применительно к 100 кг природного газа масса плазмообразующего газа составит:

6. Определяем количество не прореагировавшего метана, кг
![]()
7. Определяем количество и состав пирогаза (Табл. 2)
|
Компонент |
Количество, кг |
Количество, м3 |
Количество, % об |
|
Ацетилен Водород Этилен Метан Двуокись углерода Азот Итого |
59,437 22,006 4,413 9,246 2,966 0,629 98,697 |
51,207 246,467 3,53 12,944 1,51 0,503 316,161 |
16,19 77,96 1,12 4,09 0,48 0,16 100 |
8. Составляем сводную таблицу материального баланса (Табл. 3)
|
Приход |
Расход |
||||
|
Компонент |
Количество, кг |
Количество, масс |
Компонент |
Количество, кг |
Количество, масс |
|
Природный газ Плазмообразующий газ Итого |
100,00 6,647 106,647 |
93,8 6,2 100,00 |
Пирогаз Сажа |
98,697 5,853 104,55 |
94,4 5,6 100,00 |
Невязка: 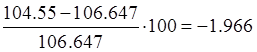
Следует отметить, что расчетный состав пирогаза и количество сажи в продуктах пиролиза удовлетворительно совпадают с экспериментальными даннымиJ
Расчет теплового баланса.
Расчет ведется на 5 плазмотронов и 5 плазмохимических реакторов.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.