Билет №12
1. Укажите кислотные центры в молекуле адреналина и расположите их в порядке уменьшения кислотных свойств.
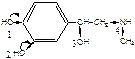
Кислотный центр – атом, соединенный с Н.
У атома азота (N) повышена ē плотность за счет электроакцепторных свойств, а также за счет электродонорных свойств группы СН3.
Чем более деполяризована ē пара тем стабильнее анион, а следственн тем сильнее кислотные свойства.
ē плотность на атоме азота повышена, поэтому атом азота проявляет основные свойства.
Больше всего ē плотность деполяризована на гидроксильных группах, связанных с бензольным кольцом за счет проявления мезомерного эффекта, поэтому они и являются главными кислотными центрами.
2. Напишите реакцию превращения, происходящую с 2- метилпропаналем в щелочной среде. Объясните причину протекания реакции.
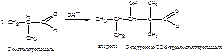
Под действием оснований водород от α-углеродного атома отщепляется собразованием карбаниона, который является нуклеофилом по отношению к карбонильной группе другой молекулы альдегида. А далее одна молекула альдегида присоединяется к оксогруппе другой молекулы.
3. Какой вид таутомерии характерен для 5-этил-5-фенил-барбитуровой кислоты. Напишите таутомерные формы и объясните причину таутомерии
Для 5-этил-5-фенилбарбитуровой кислоты невозможна кето-енольная таутомерия, т.к. для барбитуратов характерна только лактим-лактамная таутомерия.
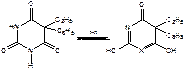
Таутомерия – это сосуществование изомерных форм, находящихся в равновесии и способных легко переходить друг в друга – динамическая изомерия.
Это выгодно с энергетической точки зрения т.к. увеличивает энтропию S.
4. Напишите реакции, протекающие при мутаротации 2-дезокси-Д-рибозы. Назовите таутомерные формы. Объсните причины и сущность мутаротации.
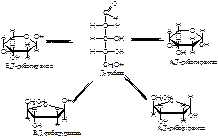
Причиной мутаротации является подвижность атома водорода.
Мутаротация – это изменение удельного угла вращения плоскополяризованного луча света во времени свежеприготовленными растворами моносахаридов.
Химический смысл заключается в том, что твердый моносахарид содержит только одну циклическую форму. При растворении через открытую форму идет образование двух пар аномеров.
5. Напишите реакцию получения О-метил-2,3,4,6-тетраметил- β,Д-маннопиранозида. Проведите гидролиз полученного соединения. Укажите условия гидролиза.
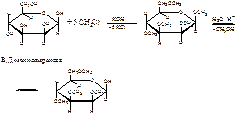 Гидролитическому
расщеплению подверглись гликозидные связи. Они – наиболее реакционноспособные.
Гидролитическому
расщеплению подверглись гликозидные связи. Они – наиболее реакционноспособные.
Гидролиз проходит в кислой среде.
6. Дайте определение понятиям: ассиметрический атом углерода, энантиомеры, эпимеры, (с примерами).
Асимметрический атом углерода – sp3-гибридизованный атом углерода, имеющий четыре различных заместителя.
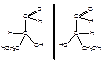
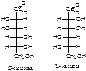 Энантиомеры –
оптические изомеры, относящиеся друг к другу, как предмет своего зеркального
отражения и имеющие одинаковые химические и физические свойства (кроме знака
вращения).
Энантиомеры –
оптические изомеры, относящиеся друг к другу, как предмет своего зеркального
отражения и имеющие одинаковые химические и физические свойства (кроме знака
вращения).
Аномеры – это диастереомеры, которые отличаются положением полуацетального гидроксила (α-β) у С*1.
![]()
Билет №12
1. Укажите кислотные центры в молекуле адреналина и расположите их в порядке уменьшения кислотных свойств.
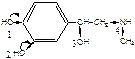
Кислотный центр – атом, соединенный с Н.
У атома азота (N) повышена ē плотность за счет электроакцепторных свойств, а также за счет электродонорных свойств группы СН3.
Чем более деполяризована ē пара тем стабильнее анион, а следственн тем сильнее кислотные свойства.
ē плотность на атоме азота повышена, поэтому атом азота проявляет основные свойства.
Больше всего ē плотность деполяризована на гидроксильных группах, связанных с бензольным кольцом за счет проявления мезомерного эффекта, поэтому они и являются главными кислотными центрами.
2. Напишите реакцию превращения, происходящую с 2- метилпропаналем в щелочной среде. Объясните причину протекания реакции.
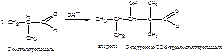
Под действием оснований водород от α-углеродного атома отщепляется собразованием карбаниона, который является нуклеофилом по отношению к карбонильной группе другой молекулы альдегида. А далее одна молекула альдегида присоединяется к оксогруппе другой молекулы.
3. Какой вид таутомерии характерен для 5-этил-5-фенил-барбитуровой кислоты. Напишите таутомерные формы и объясните причину таутомерии
Для 5-этил-5-фенилбарбитуровой кислоты невозможна кето-енольная таутомерия, т.к. для барбитуратов характерна только лактим-лактамная таутомерия.
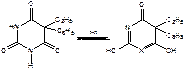
Таутомерия – это сосуществование изомерных форм, находящихся в равновесии и способных легко переходить друг в друга – динамическая изомерия.
Это выгодно с энергетической точки зрения т.к. увеличивает энтропию S.
4. Напишите реакции, протекающие при мутаротации 2-дезокси-Д-рибозы. Назовите таутомерные формы. Объсните причины и сущность мутаротации.
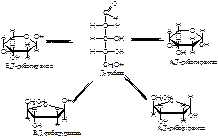
Причиной мутаротации является подвижность атома водорода.
Мутаротация – это изменение удельного угла вращения плоскополяризованного луча света во времени свежеприготовленными растворами моносахаридов.
Химический смысл заключается в том, что твердый моносахарид содержит только одну циклическую форму. При растворении через открытую форму идет образование двух пар аномеров.
5. Напишите реакцию получения О-метил-2,3,4,6-тетраметил- β,Д-маннопиранозида. Проведите гидролиз полученного соединения. Укажите условия гидролиза.
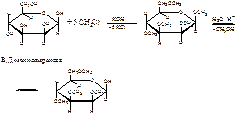 Гидролитическому
расщеплению подверглись гликозидные связи. Они – наиболее реакционноспособные.
Гидролитическому
расщеплению подверглись гликозидные связи. Они – наиболее реакционноспособные.
Гидролиз проходит в кислой среде.
6. Дайте определение понятиям: ассиметрический атом углерода, энантиомеры, эпимеры, (с примерами).
Асимметрический атом углерода – sp3-гибридизованный атом углерода, имеющий четыре различных заместителя.
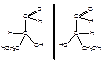
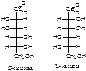 Энантиомеры –
оптические изомеры, относящиеся друг к другу, как предмет своего зеркального
отражения и имеющие одинаковые химические и физические свойства (кроме знака
вращения).
Энантиомеры –
оптические изомеры, относящиеся друг к другу, как предмет своего зеркального
отражения и имеющие одинаковые химические и физические свойства (кроме знака
вращения).
Аномеры – это диастереомеры, которые отличаются положением полуацетального гидроксила (α-β) у С*1.
![]()
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.