
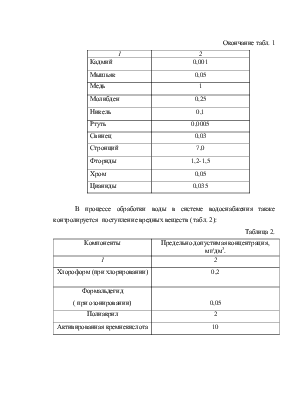
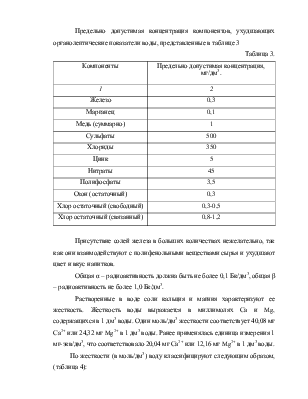









наблюдается при кипячении воды с применением перемешивания и продувания воздухом.
Гидрокарбонат магния значительно медленнее и не полностью распадается с образованием карбоната магния, растворимость которого повышается при охлаждении воды. Для удаления карбоната магния рекомендуют горячие фильтрование. При продолжительном кипячении карбонат магния гидролизуется с образованием малорастворимого гидроксида магния:
MgCO3 + H2O = Mg(OH)2 + CO2.
Этот способ даст положительный эффект в случаи превышения содержание в воде ионов кальция и магния над гидрокарбонат-ионами. Эффект умягчения и расход пара зависят от состава воды.
Ионообменный способ.
При этом способе для умягчения воды используют высокоэффективные синтетические ионообменные смолы, которые представляют собой высокополимерные, нерастворимые в воде органические вещества – гранулы полимерной смолы размером 0,5-2 мм. Обладающие способностью поглощать из раствора ионы растворенных веществ и отдавать в раствор эквивалентное количество своих ионов. Они состоят из трехмерной пространственной сетки (матрицы), содержащие ионогенные группы. В воде активные группы ионитов диссоциируют на неподвижные, связанные с матрицей ионы и подвижные противоионы.
В зависимости от знака заряда противоиона иониты подразделяются на катиониты, аниониты и амфолиты. В катионитах обменивающимся ионом является катион, в анионитах – анион, в амфолитах – ионы обоих знаков зарядов.
Катиониты применяют в основном для умягчения воды и удаления других катионов, которые содержатся в небольших количествах, а анионитами удаляют из воды кислоты и кислотные остатки. Для умягчения воды используют Н- и Na – катиониты, в которых катионы натрия и водорода обмениваются на катионы кальция и магния солей жесткости. При Н-катионировании происходят следующие реакции:
2[Кат]Н + Са(НСО3)2 = [Кат]2Са + 2СО2 + 2Н2О;
2[Кат]Н + СаCl2 = [Кат]2Са + 2НCl;
2[Кат]Н + CaSO4 = [Кат]2Са + Н2SO4.
Катионитовый фильтр представляет собой вертикальный цилиндрический сосуд с нижним и верхним сферическими днищами. Сосуд на 2/3 высоты заполнен катионитом. Внизу на бетонную подушку уложено дренажное устройство для отвода умягченной воды. Во избежание уноса мелких частиц катионита на дренажное устройство насыпан слой кварцевого песка (0,5-0,7 м) с размером зерен 1-2 мм. Вода на умягчения подается в фильтр сверху. При прохождении через слой катионита в воде протекают обменные реакции умягчения. После истощения Na-катионит регенерирует 5-10%-ным раствором хлорида натрия, а Н-катионит – 1-1,5%ной серной или 5-6%- ной соляной кислотами.
Способы обеззараживания воды.
Технологическую воду для производства безалкогольных напитков для удаления болезнетворных бактерий, содержащихся в ней, обеззараживают фильтрованием через керамические обеспложивающие фильтры, хлорированием, гораздо реже – озонированием, воздействием ультрафиолетовых лучей, обработкой ионами серебра.
Хлорирование воды.
Этот химический способ обеззараживания воды основан на бактерицидном действии кислорода. Для хлорирования используют газообразный хлор или водный раствор хлорной извести, представляющий собой смесь гипохлорита кальция Са(ОCl)2.
При растворении хлора в воде образуется хлорноватистая и соляная кислоты по уравнению (Н2О + Cl2 = HClO + HCl), а при распаде хлорноватистой кислоты отщепляется атом кислорода (HClO = HCl + O).
Соляная кислота взаимодействует с бикарбонатами, образуя нейтральные соли, в результате возрастает постоянная жесткость воды.
Доза хлора зависит от количества микроорганизмов, а также от рН, жесткости воды и содержание в ней органических веществ и колеблется
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.