В качестве характеристик, позволяющих количественно оценить результаты разделения, выступают объемные соотношения в геле.
Общий объем геля, упакованного в колонку Vt (total volume) складывается из трех величин: 1) V0 – внешний объем, объем растворителя между гранулами; 2) Vi – внутренний объем, объем растворителя внутри гранул; 3) Vm – объем матрицы, т. е. сухого геля.
Vt = V0 + Vi + Vm (15)
Vt легко определить, замерив ту часть объема колонки, в которой упакован гель. V0 определяют, пропуская через колонку высокомолекулярное вещество, неспособное проникать в гранулы. Тогда V0 равен объему элюента, сошедшего с колонки от момента нанесения такого вещества до момента его выхода с колонки.
Vi зависит от пористости геля. Значением Vm для сильно набухающих гелей можно пренебречь, тогда величину Vi можно рассчитать из формулы (15): Vi ≈ (Vt – V0).
Для веществ, которые способны проникать в гранулы геля с некоторыми затруднениями, можно оценить доступную часть внутреннего объема гранул Kav, которая не зависит от размеров колонки, но зависит от типа геля и размера молекул:
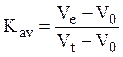 ,
(15)
,
(15)
где Ve – объем элюирования (выхода с колонки) данного вещества.
Используя Ve и ширину пика ω (см. рис. 5), можно также по уравнению (10) рассчитать число эквивалентных теоретических тарелок. Затем по формуле (11) можно определить величину ВЭТТ, оценивающую эффективность гель-фильтрации на конкретной колонке.
1. Рекомендуется выполнить их за одно практическое занятие.
2. Приступать к выполнению этих работ следует только с чистыми руками.
3. Старайтесь не касаться пальцами того участка бумаги или пластинки, где будет происходить процесс хроматографирования.
4. Используйте для разметки листа бумаги или пластинки только простые карандаши (а не ручки), а также чистые линейки и ножницы.
5. Для идентификации компонентов смеси используют метод хроматографии со свидетелями – чистыми веществами, предположительно входящими в состав разделяемой смеси. Растворы свидетелей наносят на тот же лист бумаги или пластинку, что и смесь, и хроматографируют их совместно, в одинаковых условиях.
6. Хроматография должна происходить в герметичной камере, при полной насыщенности атмосферы парами растворителя. В противном случае может иметь место так называемый эффект фитиля – растворитель с постоянной скоростью всасывается сорбентом, но фронт после достижения некоторого положения замедляет свое движение, так как происходит интенсивное испарение растворителя в атмосферу. При этом не только замедляется процесс разделения, но оно еще и ухудшается из-за подтягивания пятен к фронту.
Х-1. Разделение смеси аминокислот методом хроматографии на бумаге
Приборы и реактивы
1. Хроматографическая камера.
2. Хроматографическая бумага FN-3, листы 550 х 150 мм.
3. Капилляры из тонких стеклянных трубок для нанесения растворов веществ.
4. Простые карандаши, линейка, ножницы.
5. Система растворителей: 4 объема н-бутилового спирта (чда), 1 объем уксусной кислоты (ледяной) и 5 объемов воды. Смесь тщательно встряхивают, выдерживают не менее 48 часов, затем отделяют и используют верхний органический слой.
6. Проявитель: 0,2% раствор нингидрина в этаноле.
7. Исследуемый раствор смеси аминокислот. Концентрация каждой аминокислоты 1%.
8. Водные 1% растворы свидетелей: глицина, аланина, валина, аспарагиновой кислоты.
Смесь нескольких аминокислот может быть разделена при помощи одномерной хроматографии на бумаге. Разделение происходит вследствие различия у разных аминокислот коэффициентов распределения a между водной фазой, неподвижно закрепленной в порах бумаги, и подвижной фазой какого-либо органического растворителя. Глицин, аланин и валин относятся к группе алифатических аминокислот, а аспарагиновая кислота – к группе кислых аминокислот.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.