Однако во многоэлектронном атоме следует
учитывать не только взаимодействие электронов с ядром, но и их взаимодействие
между собой. Электронную оболочку можно рассматривать как слой, заполненный
электрическим зарядом, равным по величине сумме зарядов всех электронов данной
оболочки. Внешние электроны практически не действуют на электроны внутренних
оболочек. Действие же внутренних оболочек приводит к тому, что рассматриваемый
электрон движется в поле «нового» ядра ![]() ,
где
,
где ![]() – разность между порядковым номером
атома и числом электронов, внутренних по отношению к данному электрону.
– разность между порядковым номером
атома и числом электронов, внутренних по отношению к данному электрону. ![]() называют эффективным зарядом (
называют эффективным зарядом (![]() <Z).
При учете взаимодействия электронов абсолютные значения энергии уровней
оказывается меньше величин, найденных без учета этого взаимодействия (см.
формулу 1.1). В результате энергия внешних электронов в любом атоме по порядку
величины соответствует энергии электрона в атоме водорода, и при возбуждении
внешних оболочек атомы испускают электромагнитное излучение, лежащее в
оптической области спектра.
<Z).
При учете взаимодействия электронов абсолютные значения энергии уровней
оказывается меньше величин, найденных без учета этого взаимодействия (см.
формулу 1.1). В результате энергия внешних электронов в любом атоме по порядку
величины соответствует энергии электрона в атоме водорода, и при возбуждении
внешних оболочек атомы испускают электромагнитное излучение, лежащее в
оптической области спектра.
Вследствие эффекта экранирования потенциал
электрического поля многоэлектронных атомов с увеличением расстояния
уменьшается быстрее, чем для атома водорода. Это приводит к тому, что основная
доля энергии взаимодействия электрона с ядром связана с той частью волновой
функции ![]() , которая соответствует малым
расстояниям
, которая соответствует малым
расстояниям ![]() до ядра. У электронов с
до ядра. У электронов с ![]() = 0 эта часть существенно больше, чем
у электронов с
= 0 эта часть существенно больше, чем
у электронов с ![]() = 1, а у электронов с
= 1, а у электронов с ![]() = 1 больше, чем у электронов с
= 1 больше, чем у электронов с ![]() = 2 и т.д.
= 2 и т.д.
Наглядно это можно проиллюстрировать,
воспользовавшись представлениями теории Бора, согласно которой электроны
движутся по эллиптическим орбитам, причем вытянутость эллипса тем больше, чем
меньше квантовое число ![]() , описывающее состояние
электрона (рис.1.1).
, описывающее состояние
электрона (рис.1.1).
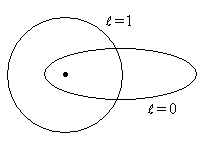
Рис. 1.1
При движении по вытянутым орбитам электроны могут ближе подходить к ядру и на некотором участке пути оказаться к ядру ближе, чем электроны внутренних по отношению к ним оболочек. В течение этого времени на них не сказывается экранирующее действие этих оболочек.
В результате во многоэлектронных атомах
происходит расщепление энергетических уровней, характеризуемых квантовым числом
п, на п – подуровней (подоболочек) с различными значениями
орбитального квантового числа ![]() . В сложных атомах
снимается вырождение по квантовому числу
. В сложных атомах
снимается вырождение по квантовому числу ![]() .
Подуровни с
.
Подуровни с ![]() =0 носят название
=0 носят название ![]() – подуровней, с
– подуровней, с ![]() =1 – р – подуровней,
=1 – р – подуровней, ![]() =2 –
=2 – ![]() –
подуровней,
–
подуровней,
![]() =3 –
=3 – ![]() – подуровней и т.д.
– подуровней и т.д.
По мере возрастания атомного номера элемента
возрастает не только количество подуровней во внешней оболочке атома, но и разница
в энергиях между ними. При этом подуровни последующей оболочки, имеющие малые
значения ![]() , могут оказаться ниже подуровней
предыдущей оболочки с большим значением
, могут оказаться ниже подуровней
предыдущей оболочки с большим значением ![]() .
.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.