Превращение арахидоновой кислоты в PG H2 происходит в шероховатом эндоплазматическом ретикулуме и катализируется циклооксигеназой (СОХ), называемой также простагландин Н2 синтазой и обладающей двумя видами активностей: циклооксигеназной и перокидазной. PG H2 является предшественником тромбоксанов и других простагландинов. Сначала под действием циклооксигеназной активности СОХ и молекулярного кислорода арахидоновая кислота превращается в нестабильное гидропероксидное производное PG G2,
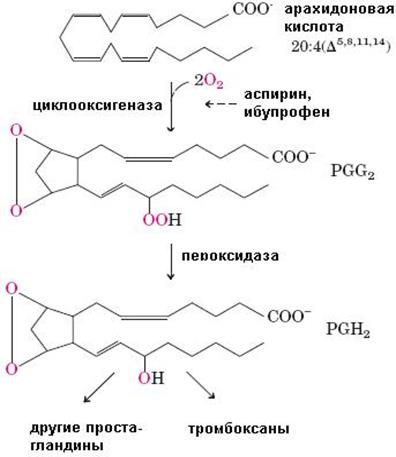 (69)
(69)
содержащее четыре атома кислорода. Гидропероксид при пятнадцатом углеродном атоме быстро восстанавливается гемом, локализованным в пероксидазном центре СОХ, до гидроксильной группы, образуя PG H2. Дальнейшие превращения PG H2 зависят от функциональной специфичности клетки. Известное противовоспалитель ное лекарство – аспирин (ацетилсалициловая кислота) ацетилирует остаток Ser530 в циклооксигеназном центре СОХ, тем самым блокируя синтез простагландинов и тромбоксанов (схема 70) и уменьшая вызываемую простагландинами воспалительную реакцию. Ибупрофен (нестероидное противовоспалительное средство) действует как конкурентный ингибитор циклооксигеназной активности СОХ.
В организме человека обнаружено две формы СОХ, имеющие близкие первичные и пространственные структуры. СОХ 1 − конститутивный фермент, используемый для синтеза простагландинов, активирующих секрецию желудочных слизей. СОХ 2, индуцируемая цитокинами изоформа, ответственна за воспалительный процесс, боль и т. д. Обе формы представляют собой гомодимеры, гидрофобные домены которых связаны с липидными мембранами эндоплазматического ретикулума (ЭР), а активные центры обращены в
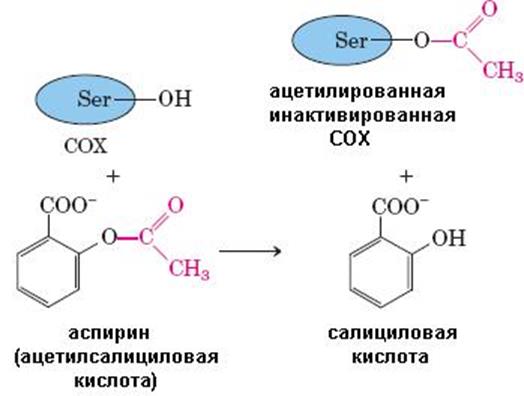 (70)
(70)
полость ЭР. На схеме 71 изображен механизм циклооксигеназной активности СОХ. Под действием тирозильного радикала в циклооксигеназном активном центре происходит отрыв протона от тринадцатого углеродного атома арахидоновой кислоты, к образовавшемуся арахидоновому радикалу (одиннадцатому углеродному атому) присоединяется первая молекула кислорода, присоединение заканчивается образованием пероксидного мостика между 9 и 11 углеродными атомами. Присоединение второй молекулы кислорода может происходить по 15 положению (путь 1 на схеме 71), или по 13 положению (путь 2).
В гладкомышечных клетках из PG H2 образуется с помощью PG Е синтазы простагландин PG Е2, а с помощью PG D синтазы простагландин PG D2. В тромбоцитах тромбоксансинтаза превращает
PG H2 в ТХ А2, действующий как сосудосуживающее средство, а вот простациклин PG I2, синтезированный из PG H2 с помощью простациклинсинтазы, наоборот, обладает сосудорасширяющим действием.
Лейкотриены
В структуре лейкотриенов, образующихся также из полиеновых кислот, отсутствуют циклы, но есть три сопряженных двойных связи
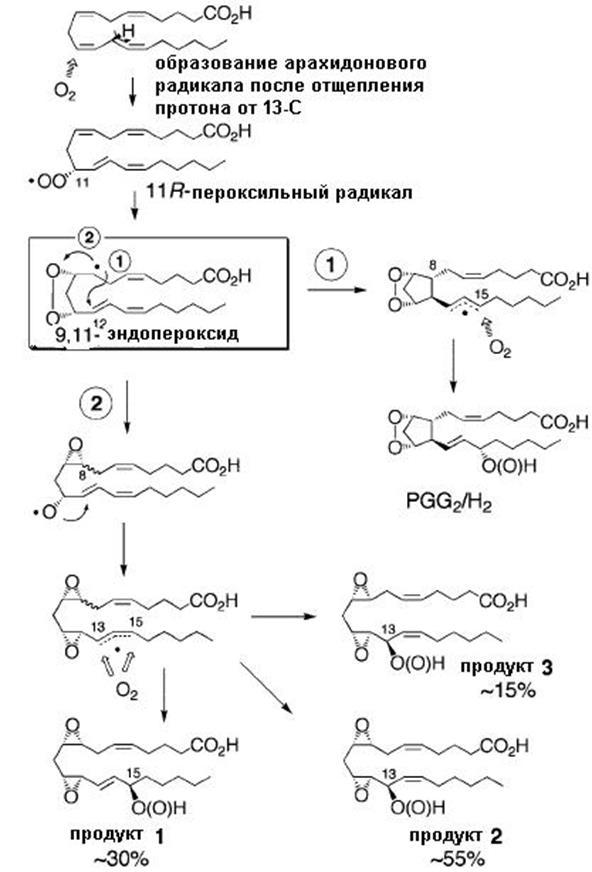 (71)
(71)
(отсюда и название лейкотриен), хотя общее количество двойных связей может быть больше. Лейкотриены C4, D4 и E4 имеют заместители в виде глутатиона, глицилцистеина и цистеина.
Синтез лейкотриенов начинается с присоединения кислорода по двойной связи у пятого, двенадцатого или пятнадцатого углеродного атома под действием липооксигеназы с образованием гидропероксидэйкозатетраеноатов (ГПЭТЕ) (схема 72). Последние или восстанавливаются до 5 (12 или 15)-гидроксиэйкозатетраеноатов (5-ГЭТЕ, 12-ГЭТЕ, 15-ГЭТЕ), или превращаются в лейкотриены. В зависимости от типа ткани липооксигеназа действует в пятом (в лейкоцитах), двенадцатом (в тромбоцитах) или пятнадцатом (в эозинофилах) положениях арахидоновой кислоты. В лейкоцитах 5-ГПЭТЕ превращается в эпоксид-лейкотриен А4 (LT A4). Его гидролиз в лейкоцитах под действием эпоксидгидролазы дает LT В4. Присоединение по шестому положению LT A4 остатка глутатиона (глутамилцистеинилглицина) с помощью глутатион-S-трансферазы приводит к образованию LT С4, удаление остатка глутаминовой кислоты из LT С4 дает LT D4, отщепление глицина нужно для образования LT Е4, который содержит только остаток цистеина.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.