6.1.8.1. Железо. В биологических объектах железо встречается в степенях окисления +2 (ферро), +3 (ферри), +4 (феррил). Предпочтительными биологическими лигандами для железа выступают атомы кислорода, азота, серы. Поэтому основные процессы в организме, в которых принимает участие железо – это транспорт и депонирование кислорода, перенос электронов по дыхательной цепи, окислительно-восстановительные реакции. Белки, содержащие железо, относятся к одной из четырех групп: железосодержащие неферментативные белки (гемоглобин, миоглобин, гемоэритрин), железо-серные ферменты (NADH-оксидоредуктаза, ксантиноксидаза, рибонуклеотидредуктаза), гем-содержащие ферменты (цитохромы, каталаза, пероксидаза, нитрооксидсинтаза), и ферменты, в которых железо не входит ни в гем, ни в железо-серный кластер (тирозингидроксилаза, пролиноксидаза) (схема 43).
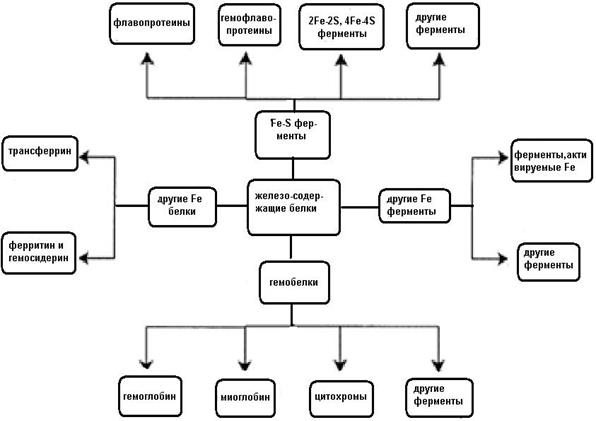 (43)
(43)
Этот элемент, как двуликий Янус, представляет для клетки и добро, и зло. Все мы хорошо знаем, что без гемоглобина, миоглобина, цитохромов и железо-серных белков невозможно существование аэробных организмов. С другой стороны, ион Fe2+ в свободном состоянии опасен для клетки, так как катализирует образование активных форм кислорода, повреждающих структурные элементы клетки и нарушающих механизмы ее функционирования (см. п. 6.1.2 данного учебного пособия и схемы 3, 24, 25).
Пути поступления железа в организм млекопитающих, в том числе человека, переносчики, способы хранения подробно рассмотрены в Части 1. Биохимия дыхания. Глава 1.3. Транспорт и депонирование железа. Здесь мы кратко напомним эти вопросы.
Железо поступает в организм в виде комплексов гемового железа, усвояемость которого высока, и негемового железа, усвояемость которого низка (всего несколько процентов от поступившего). Для переноса через апикальную мембрану клетки ион Fe3+ восстанавливается дуоденальным цитохромом B (DCYTB), ферментом, локализованным в мембране энтероцитов, и переносится транспортером дивалентных металлов 1 (divalent metal transporter 1, DMT1). Последний может транспортировать через апикальную мембрану также ионы цинка, марганца, кобальта, меди, кадмия, никеля. Для переноса
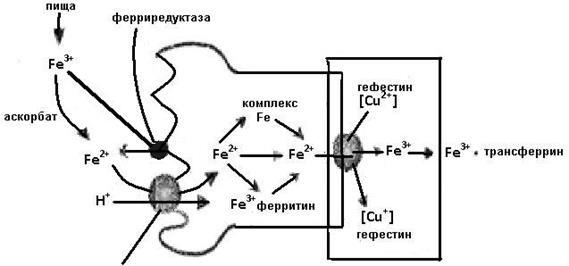
Рис. 6.19. Перенос иона железа через мембраны энтероцита в кровь
через базолатеральную мембрану энтероцита с помощью переносчика IREG 1 (iron-regulated protein 1) или ферропротеина 1 ион Fe2+ снова окисляется белком гефестином, феррооксидазой, подобной структурно и функционально церулоплазмину (медьсодержащей феррооксидазе, обнаруженной во многих тканях организма и участвующей в реакциях окисления-восстановления иона железа, связанного с ферритином). Поступив в кровь, Fe3+ взаимодействует с трансферрином (рис. 6.19) и переносится к клеткам по всему организму. Клетки, на мембранах которых есть рецепторы к трансферрину, захватывают комплекс железо-трансферрин и железо поступает внутрь клетки путем эндоцитоза. Поступившее железо может использоваться для синтеза железосодержащих белков или депонироваться в ферритине. У аэробных организмов плохо развиты системы вывода железа, поэтому в случае его избытка и невозможности депонирования в ферритине железо откладывается непосредственно в разных органах и тканях, нарушая их функционирование.
Из-за токсичности свободного железа содержание его в клетке точно регулируется на стадии трансляции мРНК ферритина и рецепторов трансферрина, содержащих в нетранслируемых областях специфические шпилечные структуры, так называемые железочувствительные элементы (IRE, iron responsive element). Связывание с этими элементами регуляторных белков регулирует количество железа в клетке: повышение потребности клеток в железе при их быстром росте или синтезе гемоглобина ведет к индукции биосинтеза рецепторов трансферрина и, напротив, при повышении запасов железа в клетке увеличивается синтез ферритина (см. Часть 1. Биохимия дыхания. Глава 1.3. Транспорт и депонирование железа).
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.