Некоторые соединения фосфора: фосфин, зарин, диизопропилфторфосфат − очень токсичны.
Зарин − изопропиловый эфир метилфторфосфоновой кислоты −
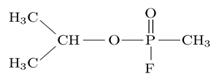
является боевым отравляющим веществом нервно-паралитического действия, вызывает поражение при любом виде воздействия, особенно быстро − при ингаляции. Зарин необратимо ингибирует фермент ацетилхолинэстеразу путём формирования ковалентного аддукта с аминокислотным остатком серина в активном центре фермента, что делает невозможным гидролиз ацетилхолина, медиато- ра, благодаря выбросу которого в межсинаптическое пространство синапса производится передача импульса к мышце или органу. В результате содержание ацетилхолина в межсинаптическом пространстве постоянно растёт, импульсы непрерывно передаются, поддерживая все иннервируемые вегетативными и двигательными нервами органы в активном состоянии вплоть до их полного истощения.
Еще одно фосфорорганическое соединение − диизопропилфторфосфат − также ингибирует ферменты, содержащие остаток серина в активном центре, в том числе и ацетилхолинэстеразу, катализирующую следующую реакцию:
|
|
Реакция происходит каждый раз после проведения нервного импульса, прежде чем второй импульс будет передан через синапс. Диизопропилфторфосфат, одно из отравляющих веществ нервно-паралитического действия, как и зарин, образуя ковалентный аддукт с остатком серина в активном центре фермента, приводит к утрате способности нейронов проводить нервные импульсы, так как модифицированный остаток серина не может более ацетилироваться ацетилхолином (рис. 6.8).
|
Рис. 6.8. Действие диизопропилфторфосфата на ацетилхолинэстеразу (АХЭ) |
6.1.5. Сера. В виде органических и неорганических соединений сера постоянно присутствует во всех живых организмах и является важным биогенным элементом. Биологическая роль серы определяется тем, что она входит в состав широко распространенных в живой природе соединений: аминокислот (метионин, цистеин, цистин, гомоцистеин), белков и пептидов; коферментов (кофермент А, липоевая кислота, S-аденозилметионин (SAM)), витаминов (биотин, тиамин), глутатиона и других. Сульфгидрилъные группы (-SH) остатков цистеина играют важную роль в структуре и каталитической активности многих ферментов. Образуя дисульфидные связи (-S-S-) внутри отдельных полипептидных цепей и между ними, эти группы участвуют в поддержании пространственной структуры молекул белков. У животных сера обнаружена также в виде органических сульфатов и сульфокислот - хондроитинсерной кислоты (в хрящах и костях), таурохолиевой кислоты (в желчи), гепарина, таурина. В некоторых железосодержащих белках (например, ферродоксинах) сера обнаружена в форме кислотолабильного сульфида. Сера способна к образованию богатых энергией связей в макроэргических соединениях, поэтому в реакциях синтеза в клетке многие соединения подвергаются активации путем образования тиоэфиров с коферментом А. Окислительно-восстановительный потенциал клетки во многом определяется соотношением тиол/дисульфид (вспомним многочисленные реакции восстановления, в которых принимает участие глутатион).
Неорганические соединения серы в организмах высших животных обнаружены в небольших количествах, главным образом в виде сульфатов (в крови, моче), а также роданидов (в слюне, желудочном соке, молоке, моче). Морские организмы богаче неорганическими соединениями серы, чем пресноводные и наземные. Для растений и многих микроорганизмов сульфат (SO42-) наряду с фосфатом и нитратом служит важнейшим источником минерального питания. Перед включением в органические соединения сера претерпевает изменения в валентности и превращается затем в органических форму в своем наименее окисленном состоянии; таким образом сера широко участвует в окислительно-восстановительных реакциях в клетках.
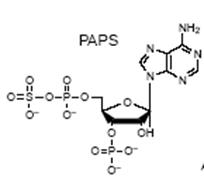 В клетках сульфаты, взаимодействуя с АТР,
превращаются в активную форму − 3’-фосфоаденозил-5’-фосфосульфат (РАРS).
В клетках сульфаты, взаимодействуя с АТР,
превращаются в активную форму − 3’-фосфоаденозил-5’-фосфосульфат (РАРS).
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.