
Министерство образования Российской Федерации
Санкт-Петербургский государственный горный институт им. Г.В. Плеханова
(технический университет)

(наименование учебной дисциплины согласно учебному плану)
Выполнил: студент гр. АПМ-03 ______________ /Зятьков Р.Э./
(подпись) (Ф.И.О.)
(подпись) (Ф.И.О.)
Санкт-Петербург
2004 год
Цель работы: построить изотерму адсорбции, проверить применимость к ней уравнений Фрейндлиха и Ленмюра, оценить удельную поверхность активированного угля.
Сущность работы: для границы раздела «твердое тело – воздух» возможно прямое экспериментальное определение удельной адсорбции, например, статическим методом. В статическом методе определяют концентрацию исходного раствора, перемешиванию навески адсорбента в каждом растворе в течении определенного времени, необходимого для установления адсорбционного равновесия , фильтрованию и определению равновесной концентрации растворенного вещества в фильтратах.
Приборы и реактивы: бюретка, мерная пипетка объемом 50 мл, мерная пипетка объемом 5 мл, колбы объемом 250 мл, колбы конические для титрования объемом 100 мл, гидроксид натрия титрованный 0,1 н раствор, фенолфталеин, раствор CH3COOH 0,4 н.
Ход работы:
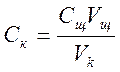 Vk=5
мл, Vщ=19 мл,
Vk=5
мл, Vщ=19 мл,
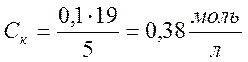 С1=0,38 моль/л
С1=0,38 моль/л 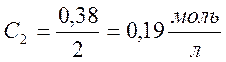 С3=0,095 моль/л
С3=0,095 моль/л
С4=0,0475 моль/л С5=0,02375 моль/л
|
|
№ |
Конц. р-ра, моль/л |
∆С=С0-С, моль/л |
m, моль/кг |
|
lgC |
lgm |
|
|
|
|
исх. С0 |
равнов. С |
||||||||
|
1 |
0,38 |
0,38 |
0 |
0 |
+ |
+ |
- |
0 |
+ |
|
2 |
0,19 |
0,14 |
0,05 |
0,83 |
0,17 |
-0,85 |
-0,08 |
7,14 |
1,2 |
|
3 |
0,095 |
0,06 |
0,035 |
0,058 |
0,1 |
-1,22 |
-0,24 |
16,7 |
1,7 |
|
4 |
0,0475 |
0,02 |
0,0275 |
0,46 |
0,043 |
-1,7 |
-0,34 |
50 |
2,3 |
|
5 |
0,02375 |
0,01 |
0,01375 |
0,23 |
0,043 |
-2 |
-0,64 |
100 |
4,3 |
С1*=С0=0,38
моль/л 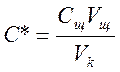
С2*=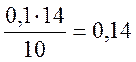 моль/л
моль/л
С3*=0,06 моль/л
С4*=0,02 моль/л
С5*=0,01 моль/л
|
|
№ |
Vk |
Vщ |
С, моль/л |
|
1 |
5 |
19 |
0,38 |
|
2 |
10 |
14 |
0,14 |
|
3 |
10 |
6 |
0,06 |
|
4 |
10 |
2 |
0,02 |
|
5 |
10 |
1 |
0,01 |
7. Вычислим
убыль концентрации кислоты в каждом растворе ∆С=С0-С, и
количество адсорбированного вещества по формуле 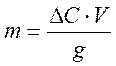 ,
где g- навеска угля:
,
где g- навеска угля:
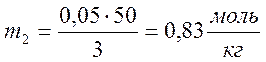
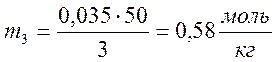
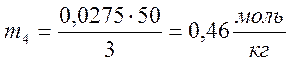
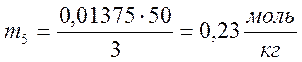
8. Изотерма адсорбции кислоты в координатах m=f(c):
9. График зависимости lgm=f(lgc)
Поскольку экспериментальные точки не укладываются на прямую, можно сделать вывод, что результаты опытов не согласуются с уравнением изотермы адсорбции Фрейндлиха.
10. График зависимости 1/m=f(1/c)
После построения зависимости 1/m=f(1/c) следует вывод о
применимости уравнения изотермы адсорбции Ленгмюра : 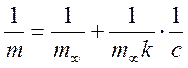 к
данному случаю адсорбции, т.к. экспериментальные точки укладываются на прямую.
к
данному случаю адсорбции, т.к. экспериментальные точки укладываются на прямую.
Константы уравнения ![]() и k определяются по размеру
соответствующих отрезков на оси координат и угловым коэффициентам:
и k определяются по размеру
соответствующих отрезков на оси координат и угловым коэффициентам:
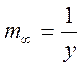 и
и 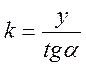
y=0,8 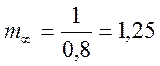
![]() tg
tg![]() =0,7
=0,7 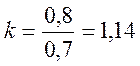
Конечный вид уравнения: 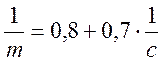
11. Вычислим удельную поверхность активированного угля по
формуле ![]() , где Na-
число Авогадро, SM- площадь поперечного
сечения молекулы адсорбата, равная для карбоновых кислот примерно 20,5.10-20
м2 .
, где Na-
число Авогадро, SM- площадь поперечного
сечения молекулы адсорбата, равная для карбоновых кислот примерно 20,5.10-20
м2 .
![]() .
.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.