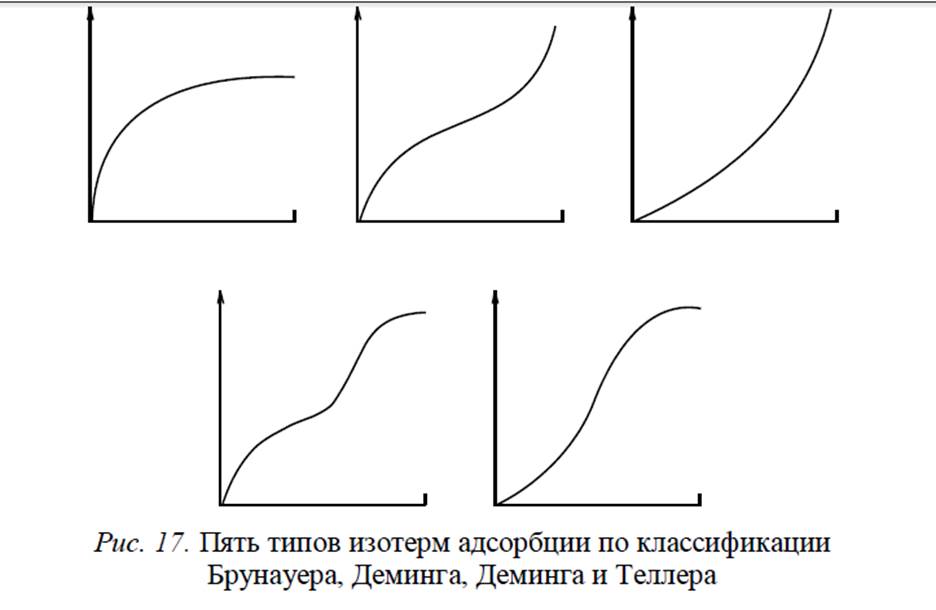
В литературе для большого ряда твердых тел приводятся десятки тысяч изотерм адсорбции. Однако все эти многочисленные изотермы, описывающие физическую адсорбцию, можно условно разбить на пять групп, соответствующих пяти группам классификации, первоначально предложенной Брунауером, Демингом, Демингом и Теллером (БДДТ). Сейчас чаще ссылаются на классификацию Брунауера, Эммета и Тел- лера (БЭТ). Эти типы изотерм показаны на рис. 17.
Классификация пор по размерам
|
Микропоры |
<20 А |
|
Мезопоры |
20A-200A |
|
Макропоры |
>200 A |
Ширина поры > глубина, то наружняя пов-ть. Если наоборот – внутренняя!
на практике удобно различать наружную и внутреннюю поверхности по правилу: внутренняя поверхность по-ристых твердых тел обычно на несколько порядков больше, чем на-ружная. Поэтому полная поверхность твердого тела будет главным образом внутренней. Однако высокодисперсные порошки многих веществ имеют большую наружную и небольшую (или даже пренебре- жимо малую) внутреннюю поверхности. Когда происходит агрегация таких частиц, то по изложенным выше причинам часть наружной по- верхности превращается во внутреннюю и образуются поры.
Термин внутренняя поверхность обычно применяется только к таким полостям, которые открыты наружу, т. е. внутренняя поверхность не включает стенки изолированных пор.
28. Адсорбция. Силы, обуславливающие адсорбцию. Теплота адсорбции.
Термин адсорбция был введен в 1881 году Кайзером для конден-сации газов на открытых поверхностях – в отличие от абсорбции га-зов, при которой молекулы газа проникают внутрь абсорбирующего твердого тела. Более широкий термин сорбция, предложенный Мак-Бейном в 1909 году, включает оба типа явлений – адсорбцию и аб-сорбцию.
Терминология
Адсорбция – самопроизв концентрир комп-тов из объема сопредельных фаз на межфазной пов-ти раздела.
Абсорбция – растворение в объеме конденсированной фазе.
Адсорбент – в-во, на кот происх адсорбц (H – host)
Адсорбат – адс-е в-во (G – guest)
Адсорбтив – еще не адсорбир G
Десорбция – удаление G из объёма или пов-ти H
Х-р взаимодействия H/G и G/G
Адсорбция вызывается действием силового поля у поверхности твердого тела (адсорбента), которое притягивает молекулы газа (ад-сорбата). Создаваемые твердым телом силы притяжения бывают в основном двух типов: физические и химические. Они обусловливают либо физическую (или ван-дер-ваальсову) адсорбцию, либо соответст-венно хемосорбцию.
Силы, обусловливающие физическую адсорбцию, всегда включают дисперсионные силы (являющиеся по природе силами притяжения) и короткодействующие силы отталкивания. Кроме того, к адсорбцион-ным силам следует отнести силы, обусловленные постоянными ди-польными моментами адсорбированных молекул.
При хемосорбции происходит переход электронов между твердым телом и адсорбированными молекулами, в результате чего образуется химическое соединение, но образуется оно только в одном слое атомов или молекул на поверхности твердого тела. Поэтому можно сказать, что в процессе хемосорбции участвуют валентные силы.
Дисперсионные силы
Свое название дисперсионные силы получили из-за того, что они обусловлены той же причиной, что и оптическая дисперсия. Эти силы, впервые описанные Лондоном, возникают в связи с тем, что быстро изменяющаяся электронная плотность в одном атоме индуцирует соответствующий электрический момент в его ближайшем соседе, что и приводит к притяжению этих двух атомов.
Чистая теплота адсорбции:
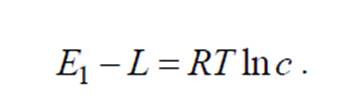
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.